
Някога се смяташе, че електроните обикалят около ядрото така, както планетите обикалят около слънцето. Тази представа отдавна е отхвърлена от съвременната квантова механика.
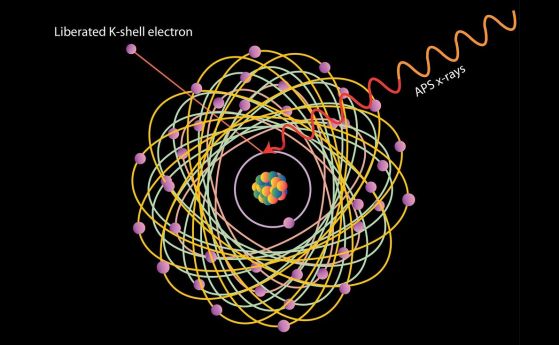
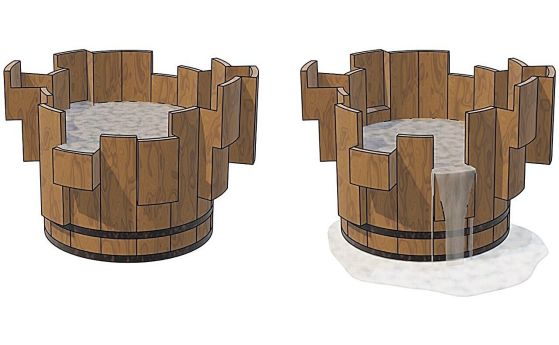
 Атомът се представя традиционно като плътно ядро, заобиколено от летящи, обикалящи го електрони. Тази картина (представена вляво) веднага води до един въпрос:
Атомът се представя традиционно като плътно ядро, заобиколено от летящи, обикалящи го електрони. Тази картина (представена вляво) веднага води до един въпрос:
Как електроните продължават да се въртят около ядрото, без да забавят ход?
Този въпрос е бил актуален в началото на 20-ти век и търсенето на отговор в крайна сметка е довело до разработването на квантовата механика.
В началото на XX век, след безброй експерименти, физиците едва започват да изграждат цялостна картина на атома. Те разбират, че всеки атом има плътно, тежко, положително заредено ядро, заобиколено от облак малки, отрицателно заредени електрони. С тази обща представа следващата им стъпка е била да създадат по-подробен модел.
При първите опити за създаване на този модел учените се вдъхновяват от Слънчевата система, която има плътно "ядро" (Слънцето), заобиколено от "облак" от по-малки частици (планетите). Този т. нар. планетарен модел обаче въвежда два съществени проблема.
От една страна, заредена частица, която се ускорява (а ускорение има винаги, когато движението не е равномерно и праволинейно - такова е движението в кръг), излъчва електромагнитно лъчение. И тъй като електроните са заредени частици и се ускоряват при движението си по орбита, те би трябвало да излъчват радиация. Това излъчване би довело до загуба на енергия на електроните, които бързо биха се завъртели в спирала и биха се сблъскали с ядрото. В началото на 1900 г. физиците са изчислили, че за да се случи подобна спирала навътре ще е нужно по-малко от една трилионна част от секундата или една пикосекунда. Тъй като атомите очевидно живеят по-дълго от една пикосекунда, това явно не се случва.
Вторият, по-дребен проблем е свързан с естеството на лъчението. Учените знаят, че атомите излъчват радиация, но с много дискретни и специфични честоти. Ако един обикалящ електрон следваше този модел на Слънчевата система, той щеше да излъчва във всякакви дължини на вълните, което противоречи на наблюденията.
Квантовото решение
Известният датски физик Нилс Бор е първият човек, който предлага решение на този проблем. През 1913 г. той изказва предположението, че електроните в атома не могат да имат каквато си поискат орбита. Вместо това те трябва да са фиксирани в орбити на много специфични разстояния от ядрото, за което му е дадена Нобелова награда. Освен това той предполага, че трябва да има минимално разстояние, което електронът може да достигне и да не се приближава повече до ядрото.
Тези идеи не идват от нищото. Малко повече от десетилетие преди това германският физик Макс Планк е предположил, че излъчването на радиация може да бъде "квантувано", което означава, че даден обект може да поглъща или излъчва радиация само на дискретни части (т.е. на порции, на кванти) и да не може да има каквато си иска стойност. Но най-малкият размер на тези дискретни парчета е константа, която става известна като константата на Планк. Преди това учените са смятали, че подобни излъчвания са непрекъснати, което означава, че частиците могат да излъчват с всякаква честота.
Константата на Планк е квант на ъгловия момент (момент на импулса) или момента на движение на обект в кръг. Така Бор пренася тази идея върху електроните, обикалящи около ядрото, като казва, че най-малката възможна орбита на електрона би била равна на ъгловия момент на точно 1 път константа на Планк. По-високите орбити биха могли да имат два пъти тази стойност, три пъти или всяко друго цяло число, кратно на константата на Планк, но никога каквато и да е част от нея (следователно не може да има 1.3 или 2.6 и т.н.).
Ще се наложи да се развие изцяло квантовата механика, за да се разбере защо електроните имат такава минимална орбита и ясно определени по-високи орбити. Електроните, както и всички частици на материята, се държат едновременно като частици и вълни. Макар че можем да си представим електрона като малка планета, която обикаля около ядрото, също толкова лесно можем да си го представим като вълна, която обгръща това ядро.
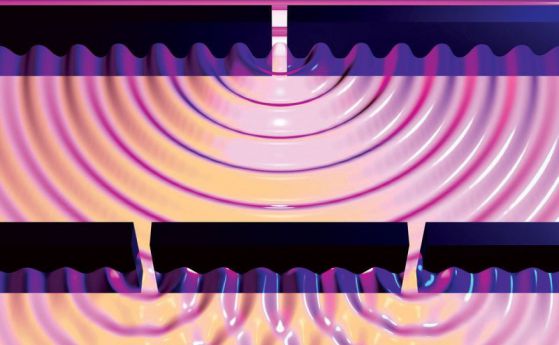
Вълните в окраничено пространство трябва да се подчиняват на специални правила. Те не могат да имат просто някаква дължина на вълната. Те трябва да са съставени от стоящи вълни, които се вписват в пространството. Точно както когато някой свири на музикален инструмент: Ако например притисне краищата на струна на китара, само определена дължина на вълните ще се впише в нея, което дава определена нота. По същия начин електронната вълна около ядрото трябва да се побере, а най-близката орбита за електрона до ядрото се дава от първата стояща вълна на този електрон.
На много опростено ниво можем да си представим електроните като стоящи вълни на материята, които имат определени допустими енергии. Шрьодингер формулира модел на атома, в който се приема, че електроните могат да се разглеждат като вълни на материята. При решаване на уравнението на Шрьодингер се получават множество вълнови функции като решения.
|
Горе: Стоящи вълни. Кредит: wikiwand
|
 Стоящи вълни в струна – основният мод и първите 5 хармоници. Кредит: wikiwand Стоящи вълни в струна – основният мод и първите 5 хармоници. Кредит: wikiwand |
В стоящата вълна по-горе, вляво, точно 7 пълни дължини на вълната се вписват в кръга. Когато обиколката на кръга не позволява цял брой дължини на вълната, възникващата деструктивна интерференция води до анулиране на вълната.
Заради принципа на неопределеност на Хайзенберг е невъзможно да се знае за даден електрон както неговото положение, така и неговата енергия. Можем само приблизително да определим местоположението на електрона, но колкото повече уточняваме местоположението му, толкова по-малко точна е информацията ни за енергията на електрона.
Вълновите функции, които се получават от уравнението на Шрьодингер за конкретен атом, се наричат още атомни орбитали. Атомната орбитала се определя като област в атома, която обхваща мястото, където електронът вероятно се намира през 90 % от времето.
Бъдещите разработки в областта на квантовата механика ще продължат да усъвършенстват тази картина, но основният момент остава: Електронът не може да се доближи до ядрото, защото квантовата му механична природа не му позволява да заема по-малко място.
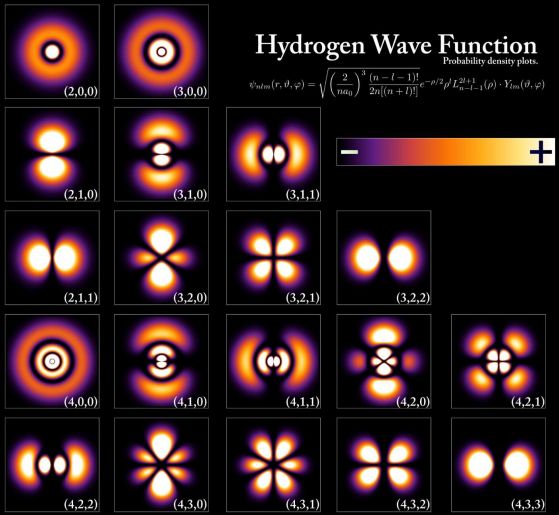 Плътност на вероятностите на електрона за първите няколко електронни орбитали на водородния атом, показани като сечения. Различните орбитали са изобразени с различен мащаб.
Плътност на вероятностите на електрона за първите няколко електронни орбитали на водородния атом, показани като сечения. Различните орбитали са изобразени с различен мащаб.
Сумиране на енергиите
Но има и съвсем различен начин за разглеждане на ситуацията, който изобщо не се основава на квантовата механика: Просто разгледайте всички участващи енергии. Електронът, който обикаля около ядро, е електрически привлечен към ядрото; той винаги се привлича към него. Но електронът има и кинетична енергия, която го кара да се отдалечава.
При стабилния атом тези две характеристики са в равновесие. Всъщност общата енергия на електрона в орбита, която е комбинация от неговата кинетична и потенциална енергия, е отрицателна. Това означава, че ако искате да премахнете електрон, трябва да добавите енергия към атома. Същото е положението и с планетите в орбита около Слънцето: За да премахнете планета от Слънчевата система, трябва да добавите енергия към системата.
Един от начините да разгледаме тази ситуация е да си представим електрон, който "пада" към ядрото, привлечен от противоположния му електрически заряд. Но поради правилата на квантовата механика той никога не може да достигне ядрото. Така че той застава в капан и вечно обикаля. Но този сценарий е разрешен от физиката, защото общата енергия на системата е отрицателна, което означава, че тя е стабилна и свързана, образувайки дълготраен атом.
Източник: Where do electrons get energy to spin around an atom's nucleus? Paul Sutter, Live Science























Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
3005
3
13.01 2023 в 22:44
18427
2
04.09 2022 в 10:57
4030
1
02.09 2022 в 17:57
Последни коментари
YKoshev
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Johnny B Goode
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Gunteer
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Християнин
Това е кралят на тиквите: Тиквата му тежи над един един тон
dolivo
Сахара очаква 75% увеличение на валежите до 2100 г.
dolivo
Земната ябълка: стара култура за новите климатични времена
dolivo
Земята потъмнява. Какво означава тази тревожна климатична тенденция за бъдещето?