

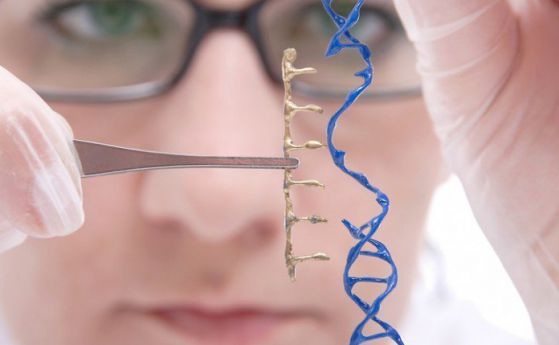
–Э–Њ–≤–∞ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є—П –љ–∞ CRISPR —Б–Є—Б—В–µ–Љ–∞—В–∞ –Ј–∞ –≥–µ–љ–љ–Њ —А–µ–і–∞–Ї—В–Є—А–∞–љ–µ –µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ –љ–∞ —Г—З–µ–љ–Є –µ—Д–µ–Ї—В–Є–≤–љ–Њ –і–∞ –Є–Ј–Љ–µ–љ—П—В –Њ—В–і–µ–ї–љ–Є –љ—Г–Ї–ї–µ–Њ—В–Є–і–љ–Є –±–∞–Ј–Є –≤ –Ф–Э–Ъ –≤ —В–Њ—З–љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ –≥–µ–љ. –Ґ–Њ–≤–∞ –њ–Њ–і–Њ–±—А–µ–љ–Є–µ –Ј–љ–∞—З–Є—В–µ–ї–љ–Њ –њ–Њ–≤–Є—И–∞–≤–∞ —Г—Б–њ–µ–≤–∞–µ–Љ–Њ—Б—В—В–∞ –љ–∞ —В–∞–Ї–Є–≤–∞ —А–µ–і–∞–Ї—Ж–Є–Є –Є –Љ–Њ–ґ–µ –і–∞ –њ–Њ–і–Њ–±—А–Є –Ј–љ–∞—З–Є—В–µ–ї–љ–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—В–∞ –љ–∞ —Г—З–µ–љ–Є—В–µ –і–∞ –Љ–Њ–і–µ–ї–Є—А–∞—В —А–∞–Ј–ї–Є—З–љ–Є —З–Њ–≤–µ—И–Ї–Є –Ј–∞–±–Њ–ї—П–≤–∞–љ–Є—П –Є –і–∞ —А–∞–Ј—А–∞–±–Њ—В–≤–∞—В –ї–µ—З–µ–љ–Є—П –Ј–∞ —В—П—Е.
–£—З–µ–љ–Є—В–µ –њ–Њ —Б–≤–µ—В–∞ –±—К—А–Ј–Њ —Б–µ –∞–і–∞–њ—В–Є—А–∞—Е–∞ –Ї—К–Љ –Љ–µ—В–Њ–і–∞ –Ј–∞ –≥–µ–љ–љ–Њ —А–µ–і–∞–Ї—В–Є—А–∞–љ–µ CRISPR-Cas9, –Ї–Њ–є—В–Њ –Є–Љ –њ–Њ–Ј–≤–Њ–ї—П–≤–∞ –Є–Ј–Ї–ї—О—З–Є—В–µ–ї–љ–Њ –ї–µ—Б–љ–Њ –і–∞ –њ—А–Њ–Љ–µ–љ—П—В –Њ–њ—А–µ–і–µ–ї–µ–љ–Є –≥–µ–љ–Є. –Т—К–њ—А–µ–Ї–Є, —З–µ –µ —Б—А–∞–≤–љ–Є—В–µ–ї–љ–Њ –ї–µ—Б–љ–Њ –і–∞ —Б–µ –Є–Ј–њ–Њ–ї–Ј–≤–∞ –Љ–µ—В–Њ–і–∞, –Ј–∞ –і–∞ —Б–µ –њ—А–µ–Ї—К—Б–љ–µ —Д—Г–љ–Ї—Ж–Є—П—В–∞ –љ–∞ –і–∞–і–µ–љ –≥–µ–љ, –Љ–љ–Њ–≥–Њ –њ–Њ-—В—А—Г–і–љ–Њ –µ –і–∞ —Б–µ –њ–Њ–њ—А–∞–≤–Є —В–Њ—З–Ї–Њ–≤–∞ –Љ—Г—В–∞—Ж–Є—П - –њ—А–Є—З–Є–љ–µ–љ–∞ –Њ—В –њ—А–Њ–Љ—П–љ–∞—В–∞ –љ–∞ –µ–і–Є–љ–Є—З–љ–∞ –±–∞–Ј–∞ –≤ –Ф–Э–Ъ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–љ–Њ—Б—В—В–∞ –љ–∞ –і–∞–і–µ–љ –≥–µ–љ - –Ї–∞—В–Њ —Б–µ –Ї–Њ—А–Є–≥–Є—А–∞ —Б–∞–Љ–Њ –≥—А–µ—И–љ–∞—В–∞ –±–∞–Ј–∞.
–Ґ–µ–Ј–Є —В–Њ—З–Ї–Њ–≤–Є –Љ—Г—В–∞—Ж–Є–Є —Б–∞ –Љ–љ–Њ–≥–Њ –≤–∞–ґ–љ–Є. "–Ю–Ї–∞–Ј–≤–∞ —Б–µ, —З–µ –±–Њ–ї—И–Є–љ—Б—В–≤–Њ—В–Њ –Њ—В –≥–µ–љ–µ—В–Є—З–љ–Є—В–µ –≤–∞—А–Є–∞–љ—В–Є, —Б–≤—К—А–Ј–∞–љ–Є —Б —З–Њ–≤–µ—И–Ї–Є –≥–µ–љ–µ—В–Є—З–љ–Є –Ј–∞–±–Њ–ї—П–≤–∞–љ–Є—П –≤—Б—К—Й–љ–Њ—Б—В —Б–∞ —В–Њ—З–Ї–Њ–≤–Є –Љ—Г—В–∞—Ж–Є–Є," —В–≤—К—А–і–Є –Ф–µ–є–≤–Є–і –Ы–Є—Г (David Liu), –±–Є–Њ—Е–Є–Љ–Є–Ї –Њ—В –•–∞—А–≤–∞—А–і—Б–Ї–Є—П —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В¬†–≤ –Ъ–µ–Љ–±—А–Є–і–ґ, —Й–∞—В–∞ –Ь–∞—Б–∞—З—Г–Ј–µ—В—Б. "–Э–Њ —Б—К–≤—А–µ–Љ–µ–љ–љ–Є—В–µ –≥–µ–љ–Њ–Љ–љ–Є –Љ–µ—В–Њ–і–Є –Ї–Њ—А–Є–≥–Є—А–∞—В —В–Њ—З–Ї–Њ–≤–Є—В–µ –Љ—Г—В–∞—Ж–Є–Є —Б –Љ–љ–Њ–≥–Њ –њ–Њ-–љ–Є—Б–Ї–∞ –µ—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В, –Њ—В–Ї–Њ–ї–Ї–Њ—В–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—В–∞ –љ–Є –і–∞ –љ–∞—А—Г—И–∞–≤–∞–Љ–µ –і–∞–і–µ–љ–Є—П –≥–µ–љ."
–Ю—В–Ї—А–Є–≤–∞–љ–µ –љ–∞ –Љ–Є—И–µ–љ–∞—В–∞
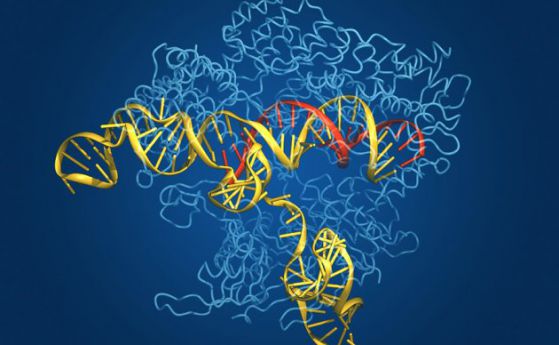
Cas9 –µ –µ–љ–Ј–Є–Љ, –Ї–Њ–є—В–Њ –Љ–Њ–ґ–µ –і–∞ —Б–µ –љ–∞—Б–Њ—З–Є –Ї—К–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ —З–∞—Б—В –Њ—В –≥–µ–љ–Њ–Љ–∞ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –≤–Њ–і–µ—Й–∞ –†–Э–Ъ –Љ–Њ–ї–µ–Ї—Г–ї–∞. –°–ї–µ–і –Ї–∞—В–Њ –Њ—В–Ї—А–Є–µ —Б—К–Њ—В–≤–µ—В—Б—В–≤–∞—Й–∞—В–∞ —Б–Є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–љ–Њ—Б—В –≤ –Ф–Э–Ъ —Б—К–≤–њ–∞–і–∞—Й–∞ —Б —В–∞–Ј–Є –≤ –†–Э–Ъ-—В–Њ, —В–Њ–є –њ—А–µ—А—П–Ј–≤–∞ –Є –і–≤–µ—В–µ –≤–µ—А–Є–≥–Є –љ–∞ –і–≤–Њ–є–љ–∞—В–∞ —Б–њ–Є—А–∞–ї–∞ —В–Њ—З–љ–Њ –љ–∞ —В–Њ–≤–∞ –Љ—П—Б—В–Њ. –Ъ–ї–µ—В–Ї–Є—В–µ —А–µ–∞–≥–Є—А–∞—В –љ–∞ —В–Њ–≤–∞ –Ї–∞—В–Њ –Ј–∞–њ–Њ—З–≤–∞—В –і–∞ –њ–Њ–њ—А–∞–≤—П—В —Б–Ї—К—Б–≤–∞–љ–µ—В–Њ, –љ–Њ –Њ–±–Є–Ї–љ–Њ–≤–µ–љ–Њ –љ–µ —Б–µ —Б–њ—А–∞–≤—П—В –Љ–љ–Њ–≥–Њ –і–Њ–±—А–µ —Б —В–Њ–≤–∞, –Ї–∞—В–Њ —З–µ—Б—В–Њ –і–Њ–±–∞–≤—П—В –Є–ї–Є –њ—А–µ–Љ–∞—Е–≤–∞—В –і–Њ–њ—К–ї–љ–Є—В–µ–ї–љ–Є –љ—Г–Ї–ї–µ–Њ—В–Є–і–Є. –Т —А–µ–Ј—Г–ї—В–∞—В –љ–∞ —В–Њ–≤–∞ –Њ–±–Є–Ї–љ–Њ–≤–µ–љ–Њ —Б–µ –љ–∞—А—Г—И–∞–≤–∞ —Д—Г–љ–Ї—Ж–Є—П—В–∞ –љ–∞ –≥–µ–љ–∞.
–£—З–µ–љ–Є—В–µ –Љ–Њ–≥–∞—В –і–∞ –Є–Ј–њ–Њ–ї–Ј–≤–∞—В –і—А—Г–≥ —В–Є–њ –њ–Њ–њ—А–∞–≤–Ї–∞, –Ї–∞—В–Њ –Њ—Б–Є–≥—Г—А—П—В –Ф–Э–Ъ –Љ–∞—В—А–Є—Ж–∞, –Ї–Њ—П—В–Њ –Ї–ї–µ—В–Ї–∞—В–∞ –Љ–Њ–ґ–µ –і–∞ –Є–Ј–њ–Њ–ї–Ј–≤–∞ –Ї–∞—В–Њ –Љ–Њ–і–µ–ї, —В–∞–Ї–∞ —З–µ –µ–љ–Ј–Є–Љ–Є—В–µ —Г—З–∞—Б—В–≤–∞—Й–Є –≤ –њ–Њ–њ—А–∞–≤–Ї–∞—В–∞ –і–∞ –і–Њ–±–∞–≤—П—В —Б—К–Њ—В–≤–µ—В—Б—В–≤–∞—Й–∞—В–∞ –Ф–Э–Ъ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–љ–Њ—Б—В –≤ –Љ—П—Б—В–Њ—В–Њ –љ–∞ —Б–Ї—К—Б–≤–∞–љ–µ. –Э–Њ —В–Њ–Ј–Є –Љ–µ—В–Њ–і –Є–Љ–∞ —Г—Б–њ–µ–≤–∞–µ–Љ–Њ—Б—В –њ–Њ-–љ–Є—Б–Ї–∞ –Њ—В 5% - –∞ –њ–Њ–љ—П–Ї–Њ–≥–∞ –і–Њ—А–Є –њ–Њ-–љ–Є—Б–Ї–∞. –Ю—Б—В–∞–љ–∞–ї–∞—В–∞ —З–∞—Б—В –Њ—В –њ–Њ–њ—А–∞–≤–Ї–Є—В–µ —Б–µ –Є–Ј–≤—К—А—И–≤–∞—В –њ–Њ –љ–µ—В–Њ—З–љ–Є—П –њ–Њ–і—Е–Њ–і.
–Ч–∞—В–Њ–≤–∞ –Ы–Є—Г –Є –µ–Ї–Є–њ—К—В –Љ—Г, –≤–Ї–ї—О—З–≤–∞—Й –±–Є–Њ—Е–Є–Љ–Є–Ї—К—В –Р–ї–µ–Ї—Б–Є—Б –Ъ–Њ–Љ–Њ—А (Alexis Komor) —Б—К—Й–Њ –Њ—В –•–∞—А–≤–∞—А–і, —Б–Є –њ–Њ—Б—В–∞–≤–Є–ї–Є –Ј–∞ —Ж–µ–ї –і–∞ –Њ—В–Ї—А–Є—П—В –љ–∞—З–Є–љ –і–∞ —А–µ–і–∞–Ї—В–Є—А–∞—В –≥–µ–љ–Њ–Љ–∞ –±–µ–Ј –і–∞ –≥–Њ –љ–∞—А—Г—И–∞–≤–∞—В. –Ґ–µ –і–µ–Ј–∞–Ї—В–Є–≤–Є—А–∞–ї–Є Cas9 –µ–љ–Ј–Є–Љ–∞, —В–∞–Ї–∞ —З–µ —В–Њ–є –і–∞ –љ–µ –Љ–Њ–ґ–µ –і–∞ –њ—А–µ—А—П–Ј–≤–∞ –Ф–Э–Ъ, —Б–ї–µ–і –Ї–Њ–µ—В–Њ –њ—А–Є–≤—К—А–Ј–∞–ї–Є –Ї—К–Љ –љ–µ–≥–Њ –і—А—Г–≥ –µ–љ–Ј–Є–Љ, –Ї–Њ–є—В–Њ –Љ–Њ–ґ–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Є –і–∞ –њ—А–µ–Њ–±—А–∞–Ј—Г–≤–∞ –µ–і–љ–∞ –љ—Г–Ї–ї–µ–Њ—В–Є–і–љ–∞ –±–∞–Ј–∞ –≤ –Ф–Э–Ъ –≤ –і—А—Г–≥–∞: —Ж–Є—В–Њ–Ј–Є–љ (–°) –≤ —Г—А–Є–і–Є–љ (U). –£—А–Є–і–Є–љ–Њ–≤–Є—В–µ –±–∞–Ј–Є –µ—Б—В–µ—Б—В–≤–µ–љ–Њ —Б–µ –Њ—В–Ї—А–Є–≤–∞—В —Б–∞–Љ–Њ –≤ –†–Э–Ъ, –љ–Њ –љ–µ –Є –≤ –Ф–Э–Ъ. –Т –Ф–Э–Ъ –Ї–ї–µ—В–Ї–∞—В–∞ –≥–Є —З–µ—В–µ –Ї–∞—В–Њ —В–Є–Љ–Є–і–Є–љ (–Ґ). –Т–Њ–і–µ—Й–∞—В–∞ –†–Э–Ъ –±–Є –љ–∞—Б–Њ—З–Є–ї–∞ –і–µ–Ј–∞–Ї—В–Є–≤–Є—А–∞–љ–Є—П Cas9 –Ї—К–Љ —Б—К–Њ—В–≤–µ—В–љ–∞—В–∞ –Љ—Г —Ж–µ–ї –≤ –≥–µ–љ–Њ–Љ–∞, –Ї—К–і–µ—В–Њ –љ–Њ–≤–Є—П—В –µ–љ–Ј–Є–Љ –њ—А–Њ–Љ–µ–љ—П –Ф–Э–Ъ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–љ–Њ—Б—В—В–∞, –≤–Љ–µ—Б—В–Њ –і–∞ —А–∞–Ј–Ї—К—Б–≤–∞ –і–≤–Њ–є–љ–Њ-—Б–њ–Є—А–∞–ї–љ–∞—В–∞ —Б—В—А—Г–Ї—В—Г—А–∞.¬†
–Ш–љ–ґ–µ–љ–µ—А–љ–Є—П—В –µ–љ–Ј–Є–Љ –Є–Љ–∞–ї 44% —Г—Б–њ–µ–≤–∞–µ–Љ–Њ—Б—В –њ—А–Є –Є–Ј–Њ–ї–Є—А–∞–љ–∞ –Ф–Э–Ъ - –Ј–љ–∞—З–Є—В–µ–ї–љ–Њ –њ–Њ–і–Њ–±—А–µ–љ–Є–µ, –Ї–Њ–µ—В–Њ —Г—З–µ–љ–Є—В–µ –і–Њ–Ї–ї–∞–і–≤–∞–ї–Є –≤ Nature. –Э–Њ –њ—А–Є –Ї–ї–µ—В–Ї–Є, –µ—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—В–∞ –±–Є–ї–∞ –љ–∞–є-–Љ–љ–Њ–≥–Њ 7,7%. –Х–і–Є–љ –Њ—В –њ—А–Њ–±–ї–µ–Љ–Є—В–µ –±–Є–ї, —З–µ –µ–љ–Ј–Є–Љ—К—В –њ—А–∞–≤–Є–ї –њ—А–Њ–Љ–µ–љ–Є —Б–∞–Љ–Њ –≤ –µ–і–љ–∞ –Њ—В –≤–µ—А–Є–≥–Є—В–µ –љ–∞ –Ф–Э–Ъ, —Б—К–Ј–і–∞–≤–∞–є–Ї–Є –љ–µ—Б—К–Њ—В–≤–µ—В—Б—В–≤–Є–µ —Б –і—А—Г–≥–∞—В–∞ –≤–µ—А–Є–≥–∞. –Я–Њ—А–∞–і–Є —В–Њ–≤–∞ –Ї–ї–µ—В–Ї–∞—В–∞ –љ–∞–є-—З–µ—Б—В–Њ –Ї–Њ—А–Є–≥–Є—А–∞–ї–∞ —В–Њ–≤–∞ –љ–µ—Б—К–Њ—В–≤–µ—В—Б—В–≤–Є–µ, –Ї–∞—В–Њ –њ—А–µ–Љ–∞—Е–≤–∞–ї–∞ –≤—К–≤–µ–і–µ–љ–∞—В–∞ –Њ—В –µ–љ–Ј–Є–Љ–∞ –Ї–Њ—А–µ–Ї—Ж–Є—П.
–Э–Њ–≤–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ
–Ы–Є—Г –Є –Ї–Њ–ї–µ–≥–Є—В–µ –Љ—Г –і–Њ–±–∞–≤–Є–ї–Є –Њ—Й–µ –µ–і–Є–љ –њ—А–Њ—В–µ–Є–љ –≤ –Є–љ–ґ–µ–љ–µ—А–љ–Є—П Cas9, –Ј–∞ –і–∞ –±–ї–Њ–Ї–Є—А–∞—В –њ—А–µ–Љ–∞—Е–≤–∞–љ–µ—В–Њ –љ–∞ U –±–∞–Ј–Є—В–µ –Њ—В –Ф–Э–Ъ –Є –љ–∞–њ—А–∞–≤–Є–ї–Є –Њ—Й–µ –љ—П–Ї–Њ–ї–Ї–Њ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є. –Я–Њ–ї—Г—З–µ–љ–∞—В–∞ –Љ–Њ–ї–µ–Ї—Г–ї–∞ "—А–µ–і–∞–Ї—В–Њ—А –љ–∞ –±–∞–Ј–Є", –Ї–∞–Ї—В–Њ —П –љ–∞—А–Є—З–∞ –Ы–Є—Г, –Ї–Њ—А–Є–≥–Є—А–∞–ї–∞ –Љ—Г—В–∞—Ж–Є–Є —Б–≤—К—А–Ј–∞–љ–Є —Б—К—Б –Ј–∞–±–Њ–ї—П–≤–∞–љ–µ—В–Њ –љ–∞ –Р–ї—Ж—Е–∞–є–Љ–µ—А –≤ –Љ–Є—И–Є –Ї–ї–µ—В–Ї–Є –Њ—В–≥–ї–µ–і–∞–љ–Є –≤ –Ї—Г–ї—В—Г—А–∞ —Б –µ—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В –і–Њ 75%, –і–Њ–Ї–ї–∞–і–≤–∞—В —Г—З–µ–љ–Є—В–µ. –†–µ–і–∞–Ї—В–Њ—А—К—В –љ–∞ –±–∞–Ј–Є –µ —Г—Б–њ—П–ї —Б—К—Й–Њ –і–∞ –Ї–Њ—А–Є–≥–Є—А–∞ –Љ—Г—В–∞—Ж–Є—П –≤ —Б–≤—К—А–Ј–∞–љ —Б —А–∞–Ї –≥–µ–љ —Б –і–Њ 7,6% –µ—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В –њ—А–Є —З–Њ–≤–µ—И–Ї–Є –Ї–ї–µ—В–Ї–Є. –°—В–∞–љ–і–∞—А—В–љ–∞—В–∞ CRISPR-Cas9 –Љ–µ—В–Њ–і–Є–Ї–∞ –Є–Ј–Њ–±—Й–Њ –љ–µ –µ —Б–њ–Њ—Б–Њ–±–љ–∞ –љ–∞ –њ–Њ–і–Њ–±–љ–Њ –љ–µ—Й–Њ.
–Ш–Љ–∞ —Б—В–Њ—В–Є—Ж–Є –і—А—Г–≥–Є –Љ—Г—В–∞—Ж–Є–Є, —Б–≤—К—А–Ј–∞–љ–Є —Б—К—Б –Ј–∞–±–Њ–ї—П–≤–∞–љ–Є—П, –Ї–Њ–Є—В–Њ –Љ–Њ–≥–∞—В –і–∞ —Б–µ –Ї–Њ—А–Є–≥–Є—А–∞—В —Б –њ–Њ–Љ–Њ—Й—В–∞ –љ–∞ –Љ–µ—В–Њ–і–∞ –Ј–∞ –њ—А–µ–≤—А—К—Й–∞–љ–µ –љ–∞ C –≤ U, —Б–Љ—П—В–∞ –Ы–Є—Г. –Х–Ї–Є–њ—К—В –Њ—В —Г—З–µ–љ–Є –≤ –Љ–Њ–Љ–µ–љ—В–∞ —Б–µ —Б—В—А–µ–Љ—П—В –і–∞ —А–∞–Ј—И–Є—А—П—В –Є–Ј—Б–ї–µ–і–≤–∞–љ–Є—П—В–∞, –Ј–∞ –і–∞ –Њ–±—Е–≤–∞–љ–∞—В –і—А—Г–≥–Є —В–Њ—З–Ї–Њ–≤–Є –Љ—Г—В–∞—Ж–Є–Є –Є –і–∞ —В–µ—Б—В–≤–∞—В —В–µ—Е–љ–Є–Ї–∞—В–∞ –њ—А–Є –ґ–Є–≤–Њ—В–љ–Є. –Ы–Є—Г —Б–µ –љ–∞–і—П–≤–∞, —З–µ –љ–µ–≥–Њ–≤–Є—В–µ –Љ–Њ–і–Є—Д–Є—Ж–Є—А–∞–љ–Є –µ–љ–Ј–Є–Љ–Є —Й–µ —Г–ї–µ—Б–љ—П—В —Б—К–Ј–і–∞–≤–∞–љ–µ—В–Њ –љ–∞ –ґ–Є–≤–Њ—В–Є–љ—Б–Ї–Є –Љ–Њ–і–µ–ї–Є, –љ–Њ—Б–µ—Й–Є —З–Њ–≤–µ—И–Ї–Є –Љ—Г—В–∞—Ж–Є–Є —Б–≤—К—А–Ј–∞–љ–Є —Б—К—Б –Ј–∞–±–Њ–ї—П–≤–∞–љ–µ—В–Њ. –Х–≤–µ–љ—В—Г–∞–ї–љ–Њ, —Б–ї–µ–і –≥–Њ–і–Є–љ–Є –љ–∞ —В–µ—Б—В–≤–∞–љ–µ –Є —Г—Б—К–≤—К—А—И–µ–љ—Б—В–≤–∞–љ–µ, –Љ–Њ–і–Є—Д–Є—Ж–Є—А–∞–љ–Є—П—В Cas9 –µ–љ–Ј–Є–Љ –Љ–Њ–ґ–µ –і–∞ —Б–µ –Є–Ј–њ–Њ–ї–Ј–≤–∞ –Є –Ј–∞ —В–µ—А–∞–њ–Є—П –љ–∞ –Ј–∞–±–Њ–ї—П–≤–∞–љ–Є—П.
–Ь–µ—В–Њ–і—К—В –Љ–Њ–ґ–µ —Б—К—Й–Њ –і–∞ —Б–µ –њ—А–Є–ї–Њ–ґ–Є –Є –њ—А–Є –і—А—Г–≥–Є –µ–љ–Ј–Є–Љ–Є. –Х–і–љ–∞ –Њ—В –∞–ї—В–µ—А–љ–∞—В–Є–≤–Є—В–µ –љ–∞ Cas9, —В. –љ–∞—А. Cpf1, –±–µ—И–µ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Є—А–∞–љ –Љ–Є–љ–∞–ї–∞—В–∞ –≥–Њ–і–Є–љ–∞ –Є –Љ–Њ–ґ–µ –і–∞ –µ –њ–Њ-–і–Њ–±—К—А –≤ –і–Њ–±–∞–≤—П–љ–µ—В–Њ –љ–∞ —Б–µ–Ї–≤–µ–љ—Ж–Є–Є –≤ –≥–µ–љ–Є—В–µ. –Ф–≤–µ –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є –Є–Ј–ї–µ–Ј–ї–Є –≤ Nature –љ–∞ 21-–≤–Є –∞–њ—А–Є–ї –і–∞–≤–∞—В –њ–Њ–≤–µ—З–µ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Ј–∞ —В–Њ–≤–∞ –Ї–∞–Ї —А–∞–±–Њ—В–Є Cpf1. –Х–і–љ–∞—В–∞ –њ–Њ–Ї–∞–Ј–≤–∞ –Ї–∞–Ї –µ–љ–Ј–Є–Љ–∞ –њ—А–Њ–Љ–µ–љ—П –Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є—П—В–∞ —Б–Є, –Ї–Њ–≥–∞—В–Њ —Б–µ —Б–≤—К—А–ґ–µ —Б –≤–Њ–і–µ—Й–∞—В–∞ –†–Э–Ъ, –∞ –і—А—Г–≥–∞—В–∞ –Њ–њ–Є—Б–≤–∞ Cpf1 –µ–љ–Ј–Є–Љ, –Ї–Њ–є—В–Њ –Љ–Њ–ґ–µ –і–∞ —Б—А—П–Ј–≤–∞ –Є –Ф–Э–Ъ, –Є –†–Э–Ъ.
–°—В–µ–љ–ї–Є –Ъ–Є (Stanley Qi), –±–Є–Њ–Є–љ–ґ–µ–љ–µ—А –Њ—В –°—В–∞–љ—Д–Њ—А–і—Б–Ї–Є—П —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В –≤ –Ъ–∞–ї–Є—Д–Њ—А–љ–Є—П —Б –љ–µ—В—К—А–њ–µ–љ–Є–µ –Њ—З–∞–Ї–≤–∞ –і–∞ –Є–Ј–њ—А–Њ–±–≤–∞ –Љ–Њ–і–Є—Д–Є—Ж–Є—А–∞–љ–Є—П Cas9 –љ–∞ –Ы–Є—Г. –Ґ–Њ–є —В–≤—К—А–і–Є, —З–µ –Љ–µ—В–Њ–і—К—В –Љ–Њ–ґ–µ –і–∞ –µ –Љ–љ–Њ–≥–Њ –њ–Њ-–њ—А–Њ—Б—В –Њ—В —Б—В–∞—А–∞—В–∞ CRISPR –Љ–µ—В–Њ–і–Є–Ї–∞, –Ї–Њ—П—В–Њ –Є–Ј–Є—Б–Ї–≤–∞ –≤–Ї–∞—А–≤–∞–љ–µ—В–Њ –љ–∞ –Ф–Э–Ъ –Љ–∞—В—А–Є—Ж–∞, –Ї–Њ—П—В–Њ –ї–µ—Б–љ–Њ –Љ–Њ–ґ–µ –і–∞ —Б–µ —А–∞–Ј–≥—А–∞–і–Є, –∞ –њ–Њ–љ—П–Ї–Њ–≥–∞ –µ –і–Њ—А–Є —В–Њ–Ї—Б–Є—З–љ–∞ –Ј–∞ –Ї–ї–µ—В–Ї–Є—В–µ. "–Ґ–Њ–≤–∞ –љ–Є –њ–Њ–Љ–∞–≥–∞ –і–∞ –Є–Ј–±–µ–≥–љ–µ–Љ —Б–µ—А–Є–Њ–Ј–љ–∞ –њ—А–µ—З–Ї–∞," –Њ–±—П—Б–љ—П–≤–∞ —В–Њ–є. "–Ґ–Њ–≤–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–Њ –±–Є —А–∞–Ј—И–Є—А–Є–ї–Њ –Њ–±—Е–≤–∞—В–∞ –љ–∞ –њ—А–Є–ї–Њ–ґ–µ–љ–Є—П—В–∞ –љ–∞ CRISPR."
–Ш–Ј—В–Њ—З–љ–Є–Ї: Nature
–Ю—Й–µ –њ–Њ —В–µ–Љ–∞—В–∞

–Ь–µ–і–Є—Ж–Є–љ–∞
–°–Р–© –Њ–і–Њ–±—А–Є—Е–∞ –≥–µ–љ–љ–Њ –Љ–Њ–і–Є—Д–Є—Ж–Є—А–∞–љ–∞ –≥—К–±–∞

–Ц–Є–≤–Њ—В—К—В
11 —З—Г–і–µ—Б–∞ –љ–∞ –Љ–µ—В–Њ–і–∞ –Ј–∞ –≥–µ–љ–љ–Њ —А–µ–і–∞–Ї—В–Є—А–∞–љ–µ CRISPR
–Ь–µ–і–Є—Ж–Є–љ–∞
–£—З–µ–љ–Є —Б–∞ –Є–Ј–њ–Њ–ї–Ј–≤–∞–ї–Є –≥–µ–љ–љ–Њ —А–µ–і–∞–Ї—В–Є—А–∞–љ–µ (CRISPR), –Ј–∞ –і–∞ –њ–Њ–њ—А–∞–≤—П—В –і–µ—Д–µ–Ї—В –њ—А–µ–і–Є–Ј–≤–Є–Ї–≤–∞—Й —Б–ї–µ–њ–Њ—В–∞

















–Ъ–Њ–Љ–µ–љ—В–∞—А–Є
–Ь–Њ–ї—П, —А–µ–≥–Є—Б—В—А–Є—А–∞–є—В–µ —Б–µ –Њ—В T–£–Ъ!
–Р–Ї–Њ –≤–µ—З–µ –Є–Љ–∞—В–µ —А–µ–≥–Є—Б—В—А–∞—Ж–Є—П, –љ–∞—В–Є—Б–љ–µ—В–µ –Ґ–£–Ъ!
–Э—П–Љ–∞ –Ї–Њ–Љ–µ–љ—В–∞—А–Є –Ї—К–Љ —В–∞–Ј–Є –љ–Њ–≤–Є–љ–∞ !
–Я–Њ—Б–ї–µ–і–љ–Є –Ї–Њ–Љ–µ–љ—В–∞—А–Є
YKoshev
–Я—А–µ—Б—В–Є–ґ–љ–∞ –љ–∞–≥—А–∞–і–∞ –Њ—В –С–Р–Э —Б–њ–µ—З–µ–ї–Є –≥–ї–∞–≤–љ–Є—П—В —А–µ–і–∞–Ї—В–Њ—А –љ–∞ –Э–∞—Г–Ї–∞OFFNews
Johnny B Goode
–Я—А–µ—Б—В–Є–ґ–љ–∞ –љ–∞–≥—А–∞–і–∞ –Њ—В –С–Р–Э —Б–њ–µ—З–µ–ї–Є –≥–ї–∞–≤–љ–Є—П—В —А–µ–і–∞–Ї—В–Њ—А –љ–∞ –Э–∞—Г–Ї–∞OFFNews
Gunteer
–Я—А–µ—Б—В–Є–ґ–љ–∞ –љ–∞–≥—А–∞–і–∞ –Њ—В –С–Р–Э —Б–њ–µ—З–µ–ї–Є –≥–ї–∞–≤–љ–Є—П—В —А–µ–і–∞–Ї—В–Њ—А –љ–∞ –Э–∞—Г–Ї–∞OFFNews
–•—А–Є—Б—В–Є—П–љ–Є–љ
–Ґ–Њ–≤–∞ –µ –Ї—А–∞–ї—П—В –љ–∞ —В–Є–Ї–≤–Є—В–µ: –Ґ–Є–Ї–≤–∞—В–∞ –Љ—Г —В–µ–ґ–Є –љ–∞–і –µ–і–Є–љ –µ–і–Є–љ —В–Њ–љ