

–Ь–∞–Ї–∞—А, —З–µ –і–Њ—Б–µ–≥–∞ –љ–Є –µ –Є–Ј–≤–µ—Б—В–µ–љ —Б–∞–Љ–Њ –Ј–µ–Љ–љ–Є—П –≤—К–≥–ї–µ—А–Њ–і–љ–Њ-–±–µ–ї—В—К—З–µ–љ-–љ—Г–Ї–ї–µ–Є–љ–Њ–≤–Њ-–≤–Њ–і–µ–љ –ґ–Є–≤–Њ—В, —В–Њ–≤–∞ –љ–µ –Њ–Ј–љ–∞—З–∞–≤–∞, —З–µ –≤ –±–µ–Ј–≥—А–∞–љ–Є—З–љ–Є—П –Ъ–Њ—Б–Љ–Њ—Б –љ–µ –Љ–Њ–ґ–µ –і–∞ —Б—К—Й–µ—Б—В–≤—Г–≤–∞—В –Є –і—А—Г–≥–Є —Д–Њ—А–Љ–Є.
–Ш–Ј–≤–µ—Б—В–љ–Є—П—В –∞—Б—В—А–Њ—Д–Є–Ј–Є–Ї –Є –Њ—Б–љ–Њ–≤–∞—В–µ–ї –љ–∞ –њ—А–Њ–≥—А–∞–Љ–∞—В–∞ SETI –Ъ–∞—А–ї –°–µ–є–≥—К–љ –Њ–±–≤–Є–љ–Є –љ–∞—Г—З–љ–Є—П —Б–≤—П—В, —З–µ –≤ —В—К—А—Б–µ–љ–µ—В–Њ –љ–∞ –Є–Ј–≤—К–љ–Ј–µ–Љ–µ–љ –ґ–Є–≤–Њ—В –Њ–±—А—К—Й–∞ –≤–љ–Є–Љ–∞–љ–Є–µ —Б–∞–Љ–Њ –љ–∞ –Њ—А–≥–∞–љ–Є—З–љ–Є—П, —В.–µ. –≤—К–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і–љ–Є—П –ґ–Є–≤–Њ—В. –Ґ–Њ–є –љ–∞—А–Є—З–∞ —В–Њ–≤–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ –≤—К–Њ–±—А–∞–ґ–µ–љ–Є–µ "–≤—К–≥–ї–µ—А–Њ–і–µ–љ —И–Њ–≤–Є–љ–Є–Ј—К–Љ" (Carbon chauvinism).
–Ф–∞–ї–Є –ґ–Є–≤–Њ—В—К—В –љ–µ –Љ–Њ–ґ–µ –і–∞ –Є–Љ–∞ —А–∞–Ј–ї–Є—З–љ–Є —Д–Њ—А–Љ–Є, –љ–∞–њ—А–Є–Љ–µ—А, –і–∞ —Б–µ –Њ—Б–љ–Њ–≤–∞–≤–∞ –љ–µ –љ–∞ –≤—К–≥–ї–µ—А–Њ–і, –∞ –љ–∞ —Б–Є–ї–Є—Ж–Є–є –Є–ї–Є –љ–∞ –і—А—Г–≥–Є –µ–ї–µ–Љ–µ–љ—В–Є?
–Ю—Б–љ–Њ–≤–∞ –љ–∞ –ґ–Є–≤–Њ—В–∞ –≤—К–≤ –Т—Б–µ–ї–µ–љ–∞—В–∞ –Љ–Њ–≥–∞—В –і–∞ –±—К–і–∞—В:
- –®–Є—А–Њ–Ї–Њ —А–∞–Ј–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—В–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Є –µ–ї–µ–Љ–µ–љ—В–Є –Њ—В IV-VII –≥—А—Г–њ–∞ –Њ—В —В–∞–±–ї–Є—Ж–∞—В–∞ –љ–∞ –Ь–µ–љ–і–µ–ї–µ–µ–≤ (–≤—К–≥–ї–µ—А–Њ–і, —Б–Є–ї–Є—Ж–Є–є, –Ї–Є—Б–ї–Њ—А–Њ–і, —Д–ї—Г–Њ—А, –∞–Ј–Њ—В, —Д–Њ—Б—Д–Њ—А, —Б—П—А–∞ –Є —В.–љ.), —Б–њ–Њ—Б–Њ–±–љ–Є –і–∞ –Њ–±—А–∞–Ј—Г–≤–∞—В —Б–ї–Њ–ґ–љ–Є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Є –≤–µ—А–Є–≥–Є –Є –і–∞ –Є–Ј–њ—К–ї–љ—П–≤–∞—В —Д—Г–љ–Ї—Ж–Є–Є—В–µ –љ–∞ –Њ—А–≥–∞–љ–Є—З–љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–Є.
- –•–Є–Љ–Є—З–µ—Б–Ї–Є—В–µ —Б—К–µ–і–Є–љ–µ–љ–Є—П (–∞–Љ–Њ–љ—П–Ї NH3, —Б–Љ–µ—Б –љ–∞ –≤–Њ–і–∞ —Б –∞–Љ–Њ–љ—П–Ї, —Б–µ—А–Њ–≤–Њ–і–Њ—А–Њ–і H2S, —Б–Є–љ–Є–ї–љ–∞ –Ї–Є—Б–µ–ї–Є–љ–∞ HCN, —Д–ї—Г–Њ—А–Њ–≤–Њ–і–Њ—А–Њ–і HF –Є —В.–і.), –Є–Љ–∞—Й–Є —Б–≤–Њ–є—Б—В–≤–Њ—В–Њ –і–∞ –±—К–і–∞—В –µ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Ї–Є—Б–µ–ї–Є–љ–∞ –Є –Њ—Б–љ–Њ–≤–∞, —Б–њ–Њ—Б–Њ–±–љ–Є –і–∞ –±—К–і–∞—В –±–Є–Њ–ї–Њ–≥–Є—З–љ–Є —А–∞–Ј—В–≤–Њ—А–Є—В–µ–ї–Є.
–Р–Љ–Њ–љ—П—З–љ–Є—П—В –ґ–Є–≤–Њ—В
–µ –≤—В–Њ—А–Є—П –њ–Њ –≤–µ—А–Њ—П—В–љ–Њ—Б—В –љ–∞ —А–∞–Ј–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П —Б–ї–µ–і –Ј–µ–Љ–љ–Є—П. –Р–Љ–Њ–љ—П–Ї—К—В –Є–Љ–∞ –і–Њ—Б—В–∞—В—К—З–љ–Њ –≤–Є—Б–Њ–Ї–∞ —В–Њ—З–Ї–∞ –љ–∞ —В–Њ–њ–µ–љ–µ, –Ї–Є–њ–µ–љ–µ –Є —В–Њ–њ–ї–Њ–µ–Љ–Ї–Њ—Б—В, –Њ—Б—В–∞–≤–∞ —В–µ—З–µ–љ –≤ –і–Є–∞–њ–∞–Ј–Њ–љ –Њ—В —В–µ–Љ–њ–µ—А–∞—В—Г—А–Є –Њ—В вАУ77,7–Њ –° –і–Њ вАУ33,4–Њ –° –њ—А–Є –љ–Њ—А–Љ–∞–ї–љ–Њ –љ–∞–ї—П–≥–∞–љ–µ, –∞ –њ—А–Є –љ–∞—А–∞—Б—В–≤–∞–љ–µ –љ–∞ –љ–∞–ї—П–≥–∞–љ–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞—В–∞ –љ–∞ –Ї–Є–њ–µ–љ–µ —Б–µ —Г–≤–µ–ї–Є—З–∞–≤–∞ (–і–Њ +132,4–Њ –° –њ—А–Є —А = 112 –∞—В–Љ). –Ю–Ї–µ–∞–љ–Є –Є –Љ–Њ—А–µ—В–∞ –Њ—В —В–µ—З–µ–љ –∞–Љ–Њ–љ—П–Ї (–Є–ї–Є —Б–Љ–µ—Б–Є –љ–∞ –∞–Љ–Њ–љ—П–Ї —Б –≤–Њ–і–∞ –Є —Е–Є–і—А–Њ–Ї—Б–Є–ї–∞–Љ–Є–љ NH2OH) –љ–µ –њ–Њ-–Ј–ї–µ –Њ—В —Е–Є–і—А–Њ—Б—Д–µ—А–∞—В–∞ –љ–∞ –Ч–µ–Љ—П—В–∞ –±–Є—Е–∞ —Б–Љ–µ–Ї—З–∞–≤–∞–ї–Є –Ї–Њ–ї–µ–±–∞–љ–Є—П—В–∞ –љ–∞ —В–µ–Љ–њ–µ—А–∞—В—Г—А–Є—В–µ. –Р–Љ–Њ–љ—П–Ї—К—В –Є–Љ–∞ –Є –љ—П–Ї–Њ–Є –±–Є–Њ–ї–Њ–≥–Є—З–љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ—А–µ–і –≤–Њ–і–∞—В–∞ (–њ–Њ-–љ–Є—Б—К–Ї –≤–Є—Б–Ї–Њ–Ј–Є—В–µ—В, —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В –і–∞ —А–∞–Ј—В–≤–∞—А—П –Њ—А–≥–∞–љ–Є—З–љ–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П –Є —В.–љ.)
–Э–Њ –∞–Ї–Њ –њ—А–Є–µ–Љ–µ–Љ –∞–Љ–Њ–љ—П–Ї—К—В –Ї–∞—В–Њ –Њ—Б–љ–Њ–≤–∞ –Ј–∞ –ґ–Є–≤–Њ—В, —В–Њ —Й–µ —Б–µ –њ–Њ—П–≤—П—В –љ—П–Ї–Њ–Є –њ—А–Њ–±–ї–µ–Љ–Є. –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞—В–∞ –Љ—Г –љ–∞ –Ї–Є–њ–µ–љ–µ –µ –і–≤–Њ–є–љ–Њ –њ–Њ-–љ–Є—Б–Ї–∞ –Њ—В —В–∞–Ј–Є –љ–∞ –≤–Њ–і–∞—В–∞, –∞ –њ–Њ–≤—К—А—Е–љ–Њ—Б—В–љ–Њ—В–Њ –Љ—Г –љ–∞–њ—А–µ–ґ–µ–љ–Є–µ –µ 3 –њ—К—В–Є –њ–Њ-–Љ–∞–ї–Ї–Њ. –Ґ–Њ–≤–∞ –Њ–Ј–љ–∞—З–∞–≤–∞, —З–µ –∞–Љ–Њ–љ—П—З–љ–Є—В–µ —Д–Њ—А–Љ–Є –љ–∞ –ґ–Є–≤–Њ—В –±–Є—Е–∞ –±–Є–ї–Є –і–Њ—Б—В–∞ –љ–µ–Њ–њ—А–µ–і–µ–ї–µ–љ–Є. –Т—К–≤ –≤—Б–µ–Ї–Є —Б–ї—Г—З–∞–є, –∞–Ї–Њ –≥–Є —Б—А–µ—Й–љ–µ–Љ вАУ —Й–µ –±—К–і–µ–Љ –Є–Ј–љ–µ–љ–∞–і–∞–љ–Є. "–Р–Љ–Њ–љ—П—З–љ–Є—П—В" –ґ–Є–≤–Њ—В –Љ–Њ–ґ–µ –і–∞ –њ—А–Њ—Ж—К—Д—В—П–≤–∞ –љ–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї–љ–Њ —Е–ї–∞–і–љ–Є –њ–ї–∞–љ–µ—В–Є –Њ—В –Ј–µ–Љ–љ–∞—В–∞ –≥—А—Г–њ–∞ –Є–ї–Є –њ–ї–∞–љ–µ—В–Њ–Є–і–Є —Б –њ–ї—К—В–љ–Є –∞—В–Љ–Њ—Б—Д–µ—А–Є.

–Ц–Є–≤–Њ—В –≤ –і—А—Г–≥–Є —А–∞–Ј—В–≤–Њ—А–Є—В–µ–ї–Є
–Я–Њ-–Љ–∞–ї–Ї–Њ –≤–µ—А–Њ—П—В–µ–љ –µ –ґ–Є–≤–Њ—В –љ–∞ –њ–Њ–≤—К—А—Е–љ–Њ—Б—В—В–∞ –љ–∞ –љ–µ–≥–Њ–ї–µ–Љ–Є –њ–ї–∞–љ–µ—В–Є —Б –∞—В–Љ–Њ—Б—Д–µ—А–Є –Њ—В –і–Є—Ж–Є–∞–љ C2N2 –Є —Е–Є–і—А–Њ—Б—Д–µ—А–Є –Њ—В —Ж–Є–∞–љ–Њ–≤–Њ–і–Њ—А–Њ–і–љ–∞ (—Б–Є–љ–Є–ї–љ–∞) –Ї–Є—Б–µ–ї–Є–љ–∞ HCN (t–Ј–∞–Љ—А—К–Ј–≤–∞–љ–µ = вАУ13,4o –°, t–Ї–Є–њ–µ–љ–µ = +25,6o –° –њ—А–Є —А = 1 –∞—В–Љ).
–Т –њ–ї—К—В–љ–Є—В–µ –∞—В–Љ–Њ—Б—Д–µ—А–Є –љ–∞ –њ–ї–∞–љ–µ—В–Є—В–µ-–≥–Є–≥–∞–љ—В–Є –≤ —Г—Б–ї–Њ–≤–Є—П—В–∞ –љ–∞ –љ–Є—Б–Ї–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–Є (–Њ—В вАУ 100o –° –і–Њ вАУ 50o –°) –Љ–Њ–ґ–µ –і–∞ –≤—К–Ј–љ–Є–Ї–љ–µ —Б–µ—А–Њ–≤–Њ–і–Њ—А–Њ–і–µ–љ –ґ–Є–≤–Њ—В. –Ц–Є–≤–Њ—В –Љ–Њ–ґ–µ –і–∞ —Б–µ –њ–Њ—П–≤–Є –Є –љ–∞ –њ–Њ–≤—К—А—Е–љ–Њ—Б—В—В–∞ –љ–∞ –њ–ї–∞–љ–µ—В–Є —Б –њ–ї—К—В–љ–Є –∞—В–Љ–Њ—Б—Д–µ—А–Є –Њ—В —Б–Љ–µ—Б –Њ—В –≥–∞–Ј–Њ–≤–µ—В–µ CS2, COS, CH4, N2, Ar, –Є —Е–Є–і—А–Њ—Б—Д–µ—А–Є –Њ—В —Б–µ—А–µ–љ –і–Є–Њ–Ї—Б–Є–і SO2 (t–Ј–∞–Љ—А—К–Ј–≤–∞–љ–µ = вАУ 75,5o –°, t–Ї–Є–њ–µ–љ–µ= вАУ 10,2o –° –њ—А–Є —А = 1 –∞—В–Љ).
–°–Є–ї–Є—Ж–Є–µ–≤ –ґ–Є–≤–Њ—В
–° –Ї–∞–Ї–≤–Њ –µ –Ј–∞–±–µ–ї–µ–ґ–Є—В–µ–ї–µ–љ —Б–Є–ї–Є—Ж–Є—П?
- –≤—В–Њ—А–Є –њ–Њ —А–∞–Ј–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –љ–∞ –Ч–µ–Љ—П—В–∞ —Б–ї–µ–і –Ї–Є—Б–ї–Њ—А–Њ–і–∞. –Я–Њ–≤–µ—З–µ –Њ—В –µ–і–љ–∞ —З–µ—В–≤—К—А—В (27,6%) –Њ—В –Љ–∞—Б–∞—В–∞ –љ–∞ –Ј–µ–Љ–љ–∞—В–∞ –Ї–Њ—А–∞ —Б–µ —Б—К—Б—В–Њ–Є –Њ—В —Б–Є–ї–Є—Ж–Є–є.
- –љ–∞–є-–±–ї–Є–Ј—К–Ї —Е–Є–Љ–Є—З–µ–љ –∞–љ–∞–ї–Њ–≥ –љ–∞ –≤—К–≥–ї–µ—А–Њ–і–∞ —Б –≤—Б–Є—З–Ї–Є –њ—А–Њ–Є–Ј—В–Є—З–∞—Й–Є –Њ—В —В–Њ–≤–∞ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П.
- –љ–∞–є-–≥–Њ–ї—П–Љ–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –љ–∞ –≤–∞–ї–µ–љ—В–љ–Њ—Б—В —Б–ї–µ–і –≤—К–≥–ї–µ—А–Њ–і–∞, –µ—Б—В–µ—Б—В–≤–µ–љ–Њ. –Ю—В –і—А—Г–≥–Є—В–µ –µ–ї–µ–Љ–µ–љ—В–Є —Б–∞–Љ–Њ –∞—В–Њ–Љ–Є—В–µ –љ–∞ —Б–Є–ї–Є—Ж–Є—П –Љ–Њ–≥–∞—В –і–∞ —Б–µ —Б—К–µ–і–Є–љ—П–≤–∞—В –µ–і–Є–љ —Б –і—А—Г–≥ —Б –Ї–Њ–≤–∞–ї–µ–љ—В–љ–Є –≤—А—К–Ј–Ї–Є.
- –Э–∞–њ—А–Є–Љ–µ—А, –њ–Њ–і–Њ–±–љ–Њ –љ–∞ –≤—К–≥–ї–µ—А–Њ–і–∞ —Б–µ –Њ–±–µ–і–Є–љ—П–≤–∞ —Б 4 –≤–Њ–і–Њ—А–Њ–і–љ–Є –∞—В–Њ–Љ–Є; –∞–љ–∞–ї–Њ–≥–Є—З–µ–љ –љ–∞ –Љ–µ—В–∞–љ–∞ (CH4) –µ —Б–Є–ї–Є—Ж–Є–µ–≤–Є—П –њ—А–Њ–і—Г–Ї—В —Б–Є–ї–∞–љ, (SiH4); —Б–Є–ї–Є–Ї–∞—В–Є—В–µ —Б–∞ –∞–љ–∞–ї–Њ–Ј–Є –љ–∞ –Ї–∞—А–±–Њ–љ–∞—В–Є—В–µ –Є —В.–љ.
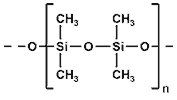
- –Ш –і–≤–∞—В–∞ –µ–ї–µ–Љ–µ–љ—В–∞ –Њ—Д–Њ—А–Љ—П—В –і—К–ї–≥–Є –≤–µ—А–Є–≥–Є, –њ–Њ–ї–Є–Љ–µ—А–Є.¬†

|
 |
 
–Э–µ–Ї–∞ –і–∞ –≥–Є —Б—А–∞–≤–љ–Є–Љ:
|
–Т—К–≥–ї–µ—А–Њ–і |
–°–Є–ї–Є—Ж–Є–є |
|
| –°–Є–Љ–≤–Њ–ї |
C |
Si |
| –Ю—В–Ї—А–Є—В |
–Я–Њ–Ј–љ–∞—В –Њ—В –і—А–µ–≤–љ–Њ—Б—В—В–∞ –Ї–∞—В–Њ "–≤—К–≥–ї–µ–љ" |
–Ю—В–і–µ–ї–µ–љ –њ—А–µ–Ј 1823–≥. –Њ—В –С–µ—А—Ж–µ–ї–Є—Г—Б |
| –С—А–Њ–є –µ–ї–µ–Ї—В—А–Њ–љ–Є |
6 |
14 |
| –У—А—Г–њ–∞ |
IV |
IV |
| –Я–Њ–ї–Њ–ґ–µ–љ–Є–µ –љ–∞ –µ–ї–µ–Ї—В—А–Њ–љ–Є—В–µ |
2s2 2p2 |
3s2 3p2 |
| –Х—Б—В–µ—Б—В–≤–µ–љ–Є –Є–Ј–Њ—В–Њ–њ–Є |
12C, |
24Si,25Si,26Si,27Si,28Si, |
| –Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ —Б—К–і—К—А–ґ–∞–љ–Є–µ |
98.9% |
92.23% |
| –Р—В–Њ–Љ–љ–Њ —В–µ–≥–ї–Њ (g/mol) |
12.0107 |
28.08550 |
| A—В–Њ–Љ–µ–љ —А–∞–і–Є—Г—Б (nm) |
0.91 |
0.146 |
| –Р–ї–Њ—В—А–Њ–њ–љ–Є —Б—К—Б—В–Њ—П–љ–Є—П | –Ї—А–Є—Б—В–∞–ї–љ–Њ, –≥—А–∞—Д–Є—В, –∞–Љ–Њ—А—Д–љ–Њ |
–Ї—А–Є—Б—В–∞–ї–љ–Њ, —В–µ—З–љ–Њ, —Б—В—К–Ї–ї–Њ–≤–Є–і–љ–Њ, –∞–Љ–Њ—А—Д–љ–Њ |
| –Я–ї—К—В–љ–Њ—Б—В (–≤ kg/m3) |
2620 |
2330 |
| –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –љ–∞ —В–Њ–њ–µ–љ–µ (¬∞C) |
3825 |
1415 |
| –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –љ–∞ –Ї–Є–њ–µ–љ–µ (¬∞C) |
4827 |
2355 |
| –°–Ї–Њ—А–Њ—Б—В –љ–∞ –Ј–≤—Г–Ї–∞ (–≤ m/s) |
18350 |
2200 |
–Э–∞ –њ—А—К–≤ –њ–Њ–≥–ї–µ–і, —Б–Є–ї–Є—Ж–Є—П—В –µ –њ–Њ–і—Е–Њ–і—П—Й –Ј–∞–Љ–µ—Б—В–љ–Є–Ї –љ–∞ –≤—К–≥–ї–µ—А–Њ–і–∞, –љ–Њ –Ї–∞–Ї–≤–Њ –Љ—Г –њ—А–µ—З–Є?
–Э—П–Ї–Њ–Є –њ—А–Њ–±–ї–µ–Љ–Є —Б—К—Б —Б–Є–ї–Є—Ж–Є–µ–≤–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј—К–Љ
–Э–µ–Ї–∞ —Б–Є –њ—А–µ–і—Б—В–∞–≤–Є–Љ –љ—П–Ї–Њ–Є –±–Є–Њ–ї–Њ–≥–Є—З–љ–Є –њ—А–Њ—Ж–µ—Б–Є —Б –≥–ї–∞–≤–µ–љ —Г—З–∞—Б—В–љ–Є–Ї —Б–Є–ї–Є—Ж–Є–є:
- –і–Є—И–∞–љ–µ—В–Њ. –Ъ–Њ–≥–∞—В–Њ –≤—К–≥–ї–µ—А–Њ–і—К—В —Б–µ –Њ–Ї–Є—Б–ї—П–≤–∞ –њ—А–Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Є—П –њ—А–Њ—Ж–µ—Б –≤ –Ј–µ–Љ–µ–љ –Њ—А–≥–∞–љ–Є–Ј—К–Љ —Б–µ –њ–Њ–ї—Г—З–∞–≤–∞ –≤—К–≥–ї–µ—А–Њ–і–µ–љ –і–Є–Њ–Ї—Б–Є–і, –Ї–Њ–є—В–Њ –µ –≥–∞–Ј –Є –ї–µ—Б–љ–Њ —Б–µ –Њ—В–і–µ–ї—П, –і–Њ–Ї–∞—В–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ—В–Њ –љ–∞ —Б–Є–ї–Є—Ж–Є—П –і–∞–≤–∞ —Б–Є–ї–Є—Ж–Є–µ–≤ –і–Є–Њ–Ї—Б–Є–і, –Ї–Њ–є—В–Њ –µ —В–≤—К—А–і–Њ —В—П–ї–Њ, –њ—А–µ–і—Б—В–∞–≤–ї—П–≤–∞—Й–Њ —А–µ—И–µ—В–Ї–∞, –≤ –Ї–Њ—П—В–Њ –≤—Б–µ–Ї–Є —Б–Є–ї–Є—Ж–Є–µ–≤ –∞—В–Њ–Љ –µ –Њ–±–Ї—А—К–ґ–µ–љ —Б —З–µ—В–Є—А–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞. –Ф–∞ —Б–µ –Њ—В—К—А–≤–∞–≤–∞—И –Њ—В –љ–µ–≥–Њ –њ—А–Є –≤—Б—П–Ї–Њ –Є–Ј–і–Є—И–≤–∞–љ–µ –±–Є –±–Є–ї–Њ —Б–µ—А–Є–Њ–Ј–љ–Њ –њ—А–µ–і–Є–Ј–≤–Є–Ї–∞—В–µ–ї—Б—В–≤–Њ.
- —Б–Є–ї–Є—Ж–Є–µ–≤–Є—В–µ —Б—К–µ–і–Є–љ–µ–љ–Є—П —Б–∞ —В—А—Г–і–љ–Њ —А–∞–Ј—В–≤–Њ—А–Є–Љ–Є –Є —Е–Є–Љ–Є—З–µ—Б–Ї–Є –Є–љ–µ—А—В–љ–Є, –Ї–∞—З–µ—Б—В–≤–∞ –≤—Б–µ –љ–µ–њ–Њ–і—Е–Њ–і—П—Й–Є –Ј–∞ –њ–Њ–і–і—К—А–ґ–∞–љ–µ –љ–∞ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –њ–Њ–љ–µ –њ—А–Є –Ј–µ–Љ–љ–Є —Г—Б–ї–Њ–≤–Є—П
–Т—К–Ј–Љ–Њ–ґ–љ–Њ –µ –і—А—Г–≥–Є –њ–ї–∞–љ–µ—В–Є –і–∞ —Б–∞ –њ–Њ-–њ–Њ–і—Е–Њ–і—П—Й–Є –Ј–∞ Si-–ґ–Є–≤–Њ—В вАУ —В–∞–Ї–Є–≤–∞, –њ—А–Є –Ї–Њ–Є—В–Њ —Б–Є–ї–Є—Ж–Є–µ–≤–Є—В–µ —Б—К–µ–і–Є–љ–µ–љ–Є—П —Б–∞ –≥–∞–Ј–Њ–Њ–±—А–∞–Ј–љ–Є –Є–ї–Є —В–µ—З–љ–Є –Є –Є–Љ–∞—В –њ–Њ-–≤–Є—Б–Њ–Ї–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–Є –Є –љ–∞–ї—П–≥–∞–љ–µ.
 
|
–Ч–∞ –і–∞ —Б–µ —А–∞–Ј–≤–Є–≤–∞—В —Д–Њ—А–Љ–Є—В–µ –љ–∞ –ґ–Є–≤–Њ—В —Б–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Є —Б–ї–Њ–ґ–љ–Є –Є —Б—В–∞–±–Є–ї–љ–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П,¬†–µ–љ–Ј–Є–Љ–Є, –±–µ–ї—В—К—Ж–Є, –Ф–Э–Ъ. –Ф–Њ–Ї–∞—В–Њ –≤—К–≥–ї–µ—А–Њ–і—К—В —Б –ї–µ–Ї–Њ—В–∞ —Б—К—Б—В–∞–≤—П –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–љ–Є —Б—В—А—Г–Ї—В—Г—А–Є (–њ—А—К—Б—В–µ–љ–Є, –і—К–ї–≥–Є –≤–µ—А–Є–≥–Є –Є –Љ–љ–Њ–≥–Њ –≤–∞–ґ–љ–Є—В–µ –і–≤–Њ–є–љ–Є —Б–њ–Є—А–∞–ї–Є), —Б–Є–ї–Є—Ж–Є—П—В –љ–µ –µ –љ–∞ —Б—К—Й–∞—В–∞ –≤–Є—Б–Њ—В–∞. –Ш–Љ–∞ –Љ–Є–ї–Є–Њ–љ —Б—В–∞–±–Є–ї–љ–Є –≤—К–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і–љ–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П, –∞ —Б–Є–ї–Є—Ж–Є–µ–≤–Є—В–µ –∞–љ–∞–ї–Њ–≥–Є—З–љ–Є —Б—В—А—Г–Ї—В—Г—А–Є —Б–∞ —Б—А–∞–≤–љ–Є—В–µ–ї–љ–Њ –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Є –Є –і–∞–ї–µ—З –љ–µ —В–∞–Ї–∞ –Љ–љ–Њ–≥–Њ–±—А–Њ–є–љ–Є вАУ —Б–∞–Љ–Њ –љ—П–Ї–Њ–ї–Ї–Њ —Б—В–Њ—В–Є–љ. |
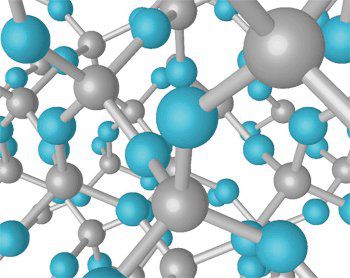 |
 
–°–Є–ї–Є—Ж–Є—П—В —Б–µ —Б—А–µ—Й–∞ —А—П–і–Ї–Њ –≤ –Ъ–Њ—Б–Љ–Њ—Б–∞
–Т—К–њ—А–µ–Ї–Є —И–Є—А–Њ–Ї–Њ—В–Њ —Б–Є —А–∞–Ј–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –љ–∞ –Ч–µ–Љ—П—В–∞, –≤—К–≤ –Т—Б–µ–ї–µ–љ–љ–∞—В–∞ —Б–Є–ї–Є—Ж–Є—П—В –µ –і–Њ—Б—В–∞ –њ–Њ-—А—П–і—К–Ї –Њ—В –≤—К–≥–ї–µ—А–Њ–і–∞ - —Ж–µ–ї–Є —Б–µ–і–µ–Љ –њ—К—В–Є.
–Р—Б—В—А–Њ–љ–Њ–Љ–Є—В–µ –љ–µ –Њ—В–Ї—А–Є–≤–∞—В —З–µ—Б—В–Њ –Љ–Њ–ї–µ–Ї—Г–ї–Є –љ–∞ —Б–Є–ї–Є—Ж–Є–є –Є–ї–Є —Б–Є–ї–Є—Ж–Є–µ–≤–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П –љ–Є—В–Њ –≤ –Љ–µ—В–µ–Њ—А–Є—В–Є—В–µ –Є –Ї–Њ–Љ–µ—В–Є—В–µ, –љ–Є—В–Њ –≤ –∞—В–Љ–Њ—Б—Д–µ—А–∞—В–∞ –љ–∞ –≥–Є–≥–∞–љ—В—Б–Ї–Є—В–µ –њ–ї–∞–љ–µ—В–Є, –≤ –Љ–µ–ґ–і—Г–Ј–≤–µ–Ј–і–љ–Њ—В–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–Њ –Є–ї–Є –≤—К–≤ –≤—К–љ—И–љ–Є—В–µ —Б–ї–Њ–µ–≤–µ –љ–∞ —Б—В—Г–і–µ–љ–Є—В–µ –Ј–≤–µ–Ј–і–Є вАУ –і–Њ–Ї–∞—В–Њ –≤—К–≥–ї–µ—А–Њ–і–љ–Є—В–µ —Б—К–µ–і–Є–љ–µ–љ–Є—П, –њ—А–Є —В–Њ–≤–∞ –Є –њ–Њ-—Б–ї–Њ–ґ–љ–Є вАУ –Ї–∞—В–Њ –≥–ї–Є—Ж–Є–љ, —Б–µ —Б—А–µ—Й–∞—В –Ј–љ–∞—З–Є—В–µ–ї–љ–Њ –њ–Њ-—З–µ—Б—В–Њ.
–Э–∞ –љ–∞—Г–Ї–∞—В–∞ —Б–∞ –Є–Ј–≤–µ—Б—В–љ–Є –Њ–Ї–Њ–ї–Њ 400 000 –љ–µ–Њ—А–≥–∞–љ–Є—З–љ–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П (–≤ —В.—З. —Б–Є–ї–Є—Ж–Є–µ–≤–Є), –љ–Њ –Њ—А–≥–∞–љ–Є—З–љ–Є—В–µ —Б—К–µ–і–Є–љ–µ–љ–Є—П —Б–∞ 8 000 000 –Є –≤—Б—П–Ї–∞ –≥–Њ–і–Є–љ–∞ —Б–µ —Г–≤–µ–ї–Є—З–∞–≤–∞—В —Б –Њ–Ї–Њ–ї–Њ 200 000 –љ–Њ–≤–Є.
 |
 |
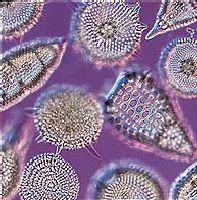 |
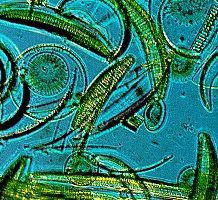
| –Ю—В –ї—П–≤–Њ –љ–∞ –і—П—Б–љ–Њ:¬†—Е–≤–Њ—Й, –і–Є–∞—В–Њ–Љ–µ–Є –Є —А–∞–і–Є–Њ–ї–∞—А–Є–Є, –љ—П–Ї–Њ–ї–Ї–Њ –Њ—В –Љ–∞–ї–Ї–Њ—В–Њ –Њ—А–≥–∞–љ–Є–Ј–Љ–Є –љ–∞ –Ч–µ–Љ—П—В–∞, —З–Є—П—В–Њ –≤—К–љ—И–љ–∞ —Б—В—А—Г–Ї—В—Г—А–∞ —Б—К–і—К—А–ґ–∞ —Б–Є–ї–Є—Ж–Є–є. |
||
–Ю—Б–љ–Њ–≤–∞—В–∞ –љ–∞ –Њ—А–≥–∞–љ–Є—З–љ–Є—П –ґ–Є–≤–Њ—В - –≤—К–≥–ї–µ—А–Њ–і—К—В –Є –≤–Њ–і–∞—В–∞ —Б–∞ –µ–і–љ–Є –Њ—В –љ–∞–є-—А–∞–Ј–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—В–µ –≤–µ—Й–µ—Б—В–≤–∞ –≤—К–≤ –Т—Б–µ–ї–µ–љ–∞—В–∞. –Ю—В 7 –љ–∞–є-—А–∞–Ј–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—В–µ –њ–Њ –Љ–∞—Б–∞ –µ–ї–µ–Љ–µ–љ—В–Є –≤ –љ–∞—И–∞—В–∞ –≥–∞–ї–∞–Ї—В–Є–Ї–∞, 4 —Б–∞ –≤ —Б—К—Б—В–∞–≤–∞ –љ–∞ –Њ—Б–љ–Њ–≤–љ–Є—В–µ –≥—А–∞–і–Є–≤–љ–Є –µ–ї–µ–Љ–µ–љ—В–Є –љ–∞ –ґ–Є–≤–Њ—В–∞ –љ–∞ –Ч–µ–Љ—П—В–∞ –Є –Ј–∞–µ–і–љ–Њ —Б –∞–Ј–Њ—В–∞ —Б–∞ 96% –Њ—В –Љ–∞—Б–∞—В–∞ –љ–∞ –љ–∞—И–µ—В–Њ —В—П–ї–Њ.
–°–Є–ї–Є—Ж–Є—П—В –љ—П–Љ–∞ –Њ–њ—В–Є—З–љ–Є –Є–Ј–Њ–Љ–µ—А–Є
–Т–∞–ґ–љ–∞ —Е–Є–Љ–Є—З–љ–∞ –Њ—Б–Њ–±–µ–љ–Њ—Б—В, –Ї–Њ—П—В–Њ –ї–Є–њ—Б–≤–∞ –њ—А–Є —Б–Є–ї–Є—Ж–Є—П –µ —Е–Є—А–∞–ї–љ–Њ—Б—В–∞, —В.–µ. –ї–Є–њ—Б–∞—В–∞ –љ–∞ –Њ–њ—В–Є—З–љ–Є –Є–Ј–Њ–Љ–µ—А–Є.
–°—К–≤—А–µ–Љ–µ–љ–љ–Њ—В–Њ –µ—Б—В–µ—Б—В–≤–Њ–Ј–љ–∞–љ–Є–µ –µ –і–Њ—Б—В–Є–≥–љ–∞–ї–Њ –і–Њ –µ–і–љ–Њ –≤–∞–ґ–љ–Њ –Њ—В–Ї—А–Є—В–Є–µ, —Б–≤—К—А–Ј–∞–љ–Њ —Б—К—Б —Б–Є–Љ–µ—В—А–Є—П—В–∞ –Є –Ї–∞—Б–∞–µ—Й–Њ —А–∞–Ј–ї–Є–Ї–Є—В–µ –Љ–µ–ґ–і—Г –ґ–Є–≤–Њ –Є –љ–µ–ґ–Є–≤–Њ. "–Ц–Є–≤–Є—В–µ" –Љ–Њ–ї–µ–Ї—Г–ї–Є, —В.–µ. –Љ–Њ–ї–µ–Ї—Г–ї–Є –љ–∞ –Њ—А–≥–∞–љ–Є—З–љ–Є—В–µ –≤–µ—Й–µ—Б—В–≤–∞, –Ї–Њ–Є—В–Њ –Є–Ј–≥—А–∞–ґ–і–∞—В –ґ–Є–≤–Є—В–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–Є —Б–∞ —А–∞–Ј–ї–Є—З–љ–Є –Њ—В "–љ–µ–ґ–Є–≤–Є—В–µ", —В.–µ. –њ–Њ–ї—Г—З–µ–љ–Є –Є–Ј–Ї—Г—Б—В–≤–µ–љ–Њ –Є —Б–∞ –Њ–≥–ї–µ–і–∞–ї–љ–Њ —Б–Є–Љ–µ—В—А–Є—З–љ–Є - –Ї–∞—В–Њ –ї—П–≤–∞ –Є –і—П—Б–љ–∞ —А—К–Ї–∞–≤–Є—Ж–∞. –Ґ–Њ–≤–∞ —Б–≤–Њ–є—Б—В–≤–Њ —Б–µ –љ–∞—А–Є—З–∞ —Е–Є—А–∞–ї–љ–Њ—Б—В. –Э–µ–ґ–Є–≤–Є—В–µ —Е–Є—А–∞–ї–љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–Є —Б–µ —Б—А–µ—Й–∞—В –≤ –њ—А–Є—А–Њ–і–∞—В–∞ –Ї–∞–Ї—В–Њ –≤ "–ї—П–≤", —В–∞–Ї–∞ –Є –≤ "–і–µ—Б–µ–љ" –≤–∞—А–Є–∞–љ—В, —В.–µ. —В–µ —Б–∞ —Е–Є—А–∞–ї–љ–Њ –љ–µ—З–Є—Б—В–Є. "–Ц–Є–≤–Є—В–µ" –Љ–Њ–ї–µ–Ї—Г–ї–Є –Љ–Њ–≥–∞—В –і–∞ –±—К–і–∞—В —Б–∞–Љ–Њ –≤ –Њ—А–Є–µ–љ—В–∞—Ж–Є—П - "–ї—П–≤–∞" –Є–ї–Є "–і—П—Б–љ–∞", —В.–µ. —В–µ —Б–∞ —Е–Є—А–∞–ї–љ–Њ —З–Є—Б—В–Є. –Э–∞–њ—А–Є–Љ–µ—А, —Б–њ–Є—А–∞–ї–∞—В–∞ –љ–∞ –µ–і–љ–∞ –Ф–Э–Ъ –Љ–Њ–ї–µ–Ї—Г–ї–∞ –µ –≤–Є–љ–∞–≥–Є –і—П—Б–љ–∞, –≥–ї—О–Ї–Њ–Ј–∞—В–∞, –Њ–±—А–∞–Ј—Г–≤–∞–љ–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –µ —Б –і—П—Б–љ–∞ —Д–Њ—А–Љ–∞, –∞ —Д—А—Г–Ї—В–Њ–Ј–∞—В–∞ - –ї—П–≤–∞.
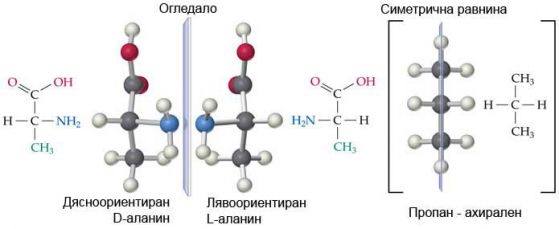
–Х—В–Њ –Ј–∞—Й–Њ, –љ–∞–є-–≤–∞–ґ–љ–∞—В–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В –љ–∞ –ґ–Є–≤–Є—В–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–Є –µ —Б—К–Ј–і–∞–≤–∞–љ–µ—В–Њ –љ–∞ —Е–Є—А–∞–ї–љ–Њ —З–Є—Б—В–Є –Љ–Њ–ї–µ–Ї—Г–ї–Є - –Є–Љ–µ–љ–љ–Њ —В–Њ–≤–∞ –Њ–њ—А–µ–і–µ–ї—П –±–Є–Њ—Е–Є–Љ–Є—З–љ–∞—В–∞ –≥—А–∞–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –ґ–Є–≤–Њ –Є –љ–µ–ґ–Є–≤–Њ.
–°—К—Й–µ—Б—В–≤—Г–≤–∞ –ї—О–±–Њ–њ–Є—В–љ–∞ —В–µ–Њ—А–Є—П, —Б–њ–Њ—А–µ–і –Ї–Њ—П—В–Њ —Б–Њ—А—В–Є—А–∞–љ–µ—В–Њ –љ–∞ –≤—К–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і–љ–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –Є–Ј–Њ–Љ–µ—А–Є—П –≤ –њ—А–µ–±–Є–Њ—В–Є—З–љ–∞—В–∞ "—Б—Г–њ–∞" –µ —Б—В–∞–≤–∞–ї–Њ –љ–∞ –њ–Њ–≤—К—А—Е–љ–Њ—Б—В—В–∞ –љ–∞ —Б–Є–ї–Є–Ї–∞—В–Є. –Ґ–∞–Ї–∞, —З–µ –∞–Ї–Њ —И–∞–љ—Б–Њ–≤–µ—В–µ –Ј–∞ —Б–Є–ї–Є—Ж–Є–µ–≤ –ґ–Є–≤–Њ—В –Љ–Њ–ґ–µ –Є –і–∞ —Б–∞ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї–љ–Є, —В–Њ —В–Њ–є –Љ–Њ–ґ–µ –і–∞ –µ –Є–Ј–Є–≥—А–∞–ї —А–µ—И–∞–≤–∞—Й–∞ —А–Њ–ї—П –њ—А–Є –≤—К–Ј–љ–Є–Ї–≤–∞–љ–µ—В–Њ –љ–∞ –≤—К–≥–ї–µ—А–Њ–і–µ–љ –ґ–Є–≤–Њ—В –љ–∞ –Ч–µ–Љ—П—В–∞.
–Э–Є–Љ–∞ —Б–Љ–µ –µ–і–Є–љ—Б—В–≤–µ–љ–Є—П—В –≤—К–≥–ї–µ—А–Њ–і–µ–љ –≤–∞—А–Є–∞–љ—В?
–Т—Б–µ –њ–∞–Ї –≤ —А–∞–Љ–Ї–Є—В–µ –љ–∞ –Њ—А–≥–∞–љ–Є—З–љ–∞—В–∞ —Е–Є–Љ–Є—П –µ–і–≤–∞ –ї–Є —Б–Љ–µ –µ–і–Є–љ—Б—В–≤–µ–љ–Є—П—В –≤–∞—А–Є–∞–љ—В. –°—К–≤—А–µ–Љ–µ–љ–љ–∞—В–∞ –љ–∞—Г–Ї–∞ –≤—Б–µ –Њ—Й–µ –љ–µ –Љ–Њ–ґ–µ –і–∞ –і–∞–і–µ —В–Њ—З–µ–љ –Њ—В–≥–Њ–≤–Њ—А –Ј–∞—Й–Њ –љ–∞—И–∞—В–∞ –Њ—А–≥–∞–љ–Є—З–љ–∞ —Д–Њ—А–Љ–∞ –љ–∞ —Б—К—Й–µ—Б—В–≤—Г–≤–∞–љ–µ –µ —В–∞–Ї–∞–≤–∞, –Ї–∞–Ї–≤–∞—В–Њ –µ –њ—А–Є –Њ–≥—А–Њ–Љ–љ–Њ—В–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –Њ—В —Б—К–µ–і–Є–љ–µ–љ–Є—П –љ–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–µ–ї–Є–љ–Є—В–µ (–≥—А–∞–і–Є–≤–љ–Є—В–µ –µ–ї–µ–Љ–µ–љ—В–Є –љ–∞ –њ—А–Њ—В–µ–Є–љ–Є—В–µ). –Э–∞–є-–≤–µ—А–Њ—П—В–љ–Њ, —В–Њ–≤–∞ –µ –њ—А–Њ—Б—В–Њ —Б–ї—Г—З–∞–є–љ–Њ. –Я—А–Є—А–Њ–і–∞—В–∞ –µ –Є–Ј–±—А–∞–ї–∞ –њ—К—А–≤–Є—П –є –њ–Њ–њ–∞–і–љ–∞–ї –Њ—В–љ–Њ—Б–Є—В–µ–ї–љ–Њ —Б—В–∞–±–Є–ї–µ–љ –≤–∞—А–Є–∞–љ—В –љ–∞ –±–Є–Њ–њ–Њ–ї–Є–Љ–µ—А –Є –љ–∞ –љ–µ–≥–Њ–≤–∞ –±–∞–Ј–∞ –µ –Ј–∞–њ–Њ—З–љ–∞–ї–∞ –і–∞ –≥—А–∞–і–Є –ґ–Є–≤–Њ—В–∞.
–Ґ–Њ–≤–∞ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–љ–Њ –≥–Њ–ї—П–Љ–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –љ–∞ –Њ—Б–љ–Њ–≤–Є –Ј–∞ –≤—К–Ј–љ–Є–Ї–≤–∞–љ–µ –љ–∞ –ґ–Є–≤–Њ—В –њ—А–Є —А–∞–Ј–ї–Є—З–љ–Є –Ї–ї–Є–Љ–∞—В–Є—З–љ–Є —Г—Б–ї–Њ–≤–Є—П.

–Я–Њ—А–∞–і–Є –≥–Њ–ї—П–Љ–Њ—В–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –Њ—В –Њ—А–≥–∞–љ–Є—З–љ–Є —Б—К–µ–і–Є–љ–µ–љ–Є—П, –ґ–Є–≤–Њ—В—К—В –љ–∞ –і—А—Г–≥–Є –њ–ї–∞–љ–µ—В–Є –Љ–Њ–ґ–µ –і–∞ –±—К–і–µ –Є –≤ –і–Њ—Б—В–∞ –њ–∞—А–∞–і–Њ–Ї—Б–∞–ї–љ–Є —Д–Њ—А–Љ–Є. –Ф–Њ—А–Є –љ–∞ —Б—К—Й–∞—В–∞ –±–Є–Њ—Е–Є–Љ–Є—З–љ–∞ –Њ—Б–љ–Њ–≤–∞, –ґ–Є–≤–Њ—В—К—В –≤ –∞–ї—В–µ—А–љ–∞—В–Є–≤–љ–Є—В–µ —Б–≤–µ—В–Њ–≤–µ –Љ–Њ–ґ–µ –і–∞ –±—К–і–µ –Є–Ј–≥—А–∞–і–µ–љ–∞ –Њ—В "–і–µ—Б–љ–Є" –∞–Љ–Є–љ–Њ–Ї–Є—Б–µ–ї–Є–љ–Є –Є "–ї–µ–≤–Є" –≤—К–≥–ї–µ—Е–Є–і—А–∞—В–Є, –∞ –љ–µ –Њ–±—А–∞—В–љ–Њ—В–Њ –Ї–∞–Ї—В–Њ –љ–∞ –Ч–µ–Љ—П—В–∞.¬†–Р —А–∞–Ј–ї–Є–Ї–∞—В–∞ –Љ–Њ–ґ–µ –і–∞ –±—К–і–µ –Љ–љ–Њ–≥–Њ –њ–Њ-–Ј–љ–∞—З–Є—В–µ–ї–љ–∞ –Њ—В —Е–Є—А–∞–ї–љ–∞—В–∞ –Њ—А–Є–µ–љ—В–∞—Ж–Є—П.
–Ъ–∞–ї—Ж–Є–є —Б—А–µ—Й—Г —Б–Є–ї–Є—Ж–Є–є
–Ф–Њ–Ї–∞—В–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—В–∞ –љ–∞ –Ї–∞–ї—Ж–Є—П –≤ –і—А–µ–≤–љ–Є—П—В –Њ–Ї–µ–∞–љ –±–Є–ї–∞ –Њ—Й–µ –љ–Є—Б–Ї–∞, —Б–Є–ї–Є—Ж–Є—П—В –µ –Є–Ј–њ—К–ї–љ—П–≤–∞–ї –Љ–љ–Њ–≥–Њ–±—А–Њ–є–љ–Є —Д—Г–љ–Ї—Ж–Є–Є, –≤ —В–Њ–≤–∞ —З–Є—Б–ї–Њ —Д—Г–љ–Ї—Ж–Є–Є—В–µ –њ–Њ —Б—К–Ј–і–∞–≤–∞–љ–µ—В–Њ –љ–∞ –њ—К—А–≤–Є—В–µ –Њ–њ–Њ—А–љ–Є, —Б–Ї–µ–ї–µ—В–љ–Є —Б—В—А—Г–Ї—В—Г—А–Є –≤ –њ—А–Є–Љ–Є—В–Є–≤–љ–Є—В–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–Є. –Т–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–µ –≥–Њ –µ –Є–Ј–Љ–µ—Б—В–Є–ї –њ–Њ-–ї–µ–Ї–Є—П –Є –ї–µ—Б–љ–Њ—А–µ–∞–≥–Є—А–∞—Й –Ї–∞–ї—Ж–Є–є. –Х—В–Њ –љ—П–Ї–Њ–ї–Ї–Њ –њ—А–Є–Љ–µ—А–∞:
- –Э–∞–є-–і—А–µ–≤–љ–Є—В–µ –≤ –µ–≤–Њ–ї—О—Ж–Є–Њ–љ–µ–љ –њ–ї–∞–љ –њ—А–Є–Љ–Є—В–Є–≤–љ–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–Є: –Љ–Њ—А—Б–Ї–Є—В–µ –≥—К–±–Є, —А–∞–і–Є–Њ–ї–∞—А–Є–Є—В–µ –Є –і–Є–∞—В–Њ–Љ–µ–Є—В–µ –Є–Љ–∞—В —Б–Є–ї–Є—Ж–Є–µ–≤ —Б–Ї–µ–ї–µ—В, –њ–Њ-–љ–∞–њ—А–µ–і–љ–∞–ї–Є—В–µ - —Б–Є–ї–Є—Ж–Є–µ–≤–Њ-–Ї–∞–ї—Ж–Є–µ–≤, –∞ –љ–∞–є-–µ–≤–Њ–ї—О—Ж–Є–Њ–љ–љ–Њ –љ–∞–њ—А–µ–і–љ–∞–ї–Є—В–µ - –Ї–∞–ї—Ж–Є–µ–≤.
 
| ¬† –Т–ї—П–≤–Њ –µ —А–∞–і–Є–Њ–ї–∞—А–Є—П, –≤–і—П—Б–љ–Њ - –і–Є–∞—В–Њ–Љ–µ–∞. |  |
 |
 
- –Ф—А—Г–≥ –њ—А–Є–Љ–µ—А —Б–∞ –љ–∞–є-–і—А–µ–≤–љ–Є—В–µ —А–Є–±–Є (–∞–Ї—Г–ї–Є, —Б–Ї–∞—В–Њ–≤–µ), —З–Є–Є—В–Њ —Б–Ї–µ–ї–µ—В–Є —Б–∞ –±–Њ–≥–∞—В–Є –љ–∞ —Б–Є–ї–Є—Ж–Є–є. –Я—А–Є –њ–Њ-–µ–≤–Њ–ї—О—Ж–Є–Њ–љ–љ–Њ –љ–∞–њ—А–µ–і–љ–∞–ї–Є—В–µ —А–Є–±–Є - –Ї–Њ—Б—В–љ–Є—В–µ - –Є–Љ–∞—В –њ–Њ–≤–µ—З–µ –Ї–∞–ї—Ж–Є–є –≤ –Ї–Њ—Б—В–Є—В–µ —Б–Є.
–Ш –љ–∞–Ї—А–∞—П - —З–Њ–≤–µ–Ї—К—В. –С–Є–Њ–≥–µ–љ–µ—В–Є—З–љ–Є—П—В –Ј–∞–Ї–Њ–љ –љ–∞ –•–µ–Ї–µ–ї –≥–ї–∞—Б–Є: –Ю–љ—В–Њ–≥–µ–љ–µ–Ј–∞—В–∞ –µ –Ї—А–∞—В–Ї–Њ –њ–Њ–≤—В–Њ—А–µ–љ–Є–µ –љ–∞ —Д–Є–ї–Њ–≥–µ–љ–µ–Ј–∞—В–∞. –° –і—А—Г–≥–Є –і—Г–Љ–Є, –≤—Б–µ–Ї–Є –ґ–Є–≤ –Њ—А–≥–∞–љ–Є–Ј—К–Љ –њ–Њ–≤—В–∞—А—П –≤ –Є–Ј–Љ–µ–љ–µ–љ–Є—П—В–∞ –љ–∞ –Ј–∞—А–Њ–і–Є—И–∞ —Б–Є –≤—Б–Є—З–Ї–Є –µ–≤–Њ–ї—О—Ж–Є–Њ–љ–Є –њ—А–Њ–Љ–µ–љ–Є –љ–∞ –њ—А–µ–і—Ж–Є—В–µ —Б–Є. –Т –Љ–љ–Њ–≥–Њ–±—А–Њ–є–љ–Є –Є–Ј—Б–ї–µ–і–≤–∞–љ–Є—П –µ —Г—Б—В–∞–љ–Њ–≤–µ–љ–Њ, —З–µ –љ–∞–є-–≤–Є—Б–Њ–Ї–∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –љ–∞ —Б–Є–ї–Є—Ж–Є–є –Є–Љ–∞ –≤ —З–Њ–≤–µ—И–Ї–Є—П –Ј–∞—А–Њ–і–Є—И, –∞ –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ –љ–∞ —А–∞–ґ–і–∞–љ–µ —В—П –њ–Њ—Б—В–µ–њ–µ–љ–Њ –љ–∞–Љ–∞–ї—П–≤–∞. –Ш –Њ—В —А–∞–ґ–і–∞–љ–µ—В–Њ –і–Њ —Б—В–∞—А–Њ—Б—В—В–∞ —Г —З–Њ–≤–µ–Ї–∞ —Б—К–Њ—В–љ–Њ—И–µ–љ–Є–µ—В–Њ –љ–∞ —Б–Є–ї–Є—Ж–Є—П –Є –Ї–∞–ї—Ж–Є—П –≤—К–≤ –≤—Б–Є—З–Ї–Є —В—К–Ї–∞–љ–Є –љ–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Њ—Б–Њ–±–µ–љ–Њ –≤ —Б—К–µ–і–Є–љ–Є—В–µ–ї–љ–Є—В–µ, —Б–µ –Є–Ј–Љ–µ–љ—П –≤ –њ–Њ–ї–Ј–∞ –љ–∞ –Ї–∞–ї—Ж–Є—П. –Т–Є—Б–Њ–Ї–∞—В–∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –љ–∞ –Ї–∞–ї—Ж–Є—П –µ –њ—А–Є—З–Є–љ–∞ –Ј–∞ –Љ–љ–Њ–≥–Њ "–±–Њ–ї–µ—Б—В–Є –љ–∞ —Ж–Є–≤–Є–ї–Є–Ј–∞—Ж–Є—П—В–∞" - –Ї—А–µ—Е–Ї–Њ—Б—В –љ–∞ –Ї–Њ—Б—В–Є—В–µ, –Ї–∞–ї—Ж–Є—А–∞–љ–µ –љ–∞ –Ї—А—К–≤–Њ–љ–Њ—Б–љ–Є—В–µ —Б—К–і–Њ–≤–µ –Є —Е—А—Г—Й—П–ї–Є—В–µ –Є –і—А.
–Ш–Ј—В–Њ—З–љ–Є–Ї:
La chimie du silicium, luxorion


















–Ъ–Њ–Љ–µ–љ—В–∞—А–Є
–Ь–Њ–ї—П, —А–µ–≥–Є—Б—В—А–Є—А–∞–є—В–µ —Б–µ –Њ—В T–£–Ъ!
–Р–Ї–Њ –≤–µ—З–µ –Є–Љ–∞—В–µ —А–µ–≥–Є—Б—В—А–∞—Ж–Є—П, –љ–∞—В–Є—Б–љ–µ—В–µ –Ґ–£–Ъ!
03.11 2015 –≤ 16:15
04.10 2015 –≤ 07:48
–§–ї—Г–Њ—А—К—В –µ –Њ—В VII –≥—А—Г–њ–∞.
03.10 2015 –≤ 17:01
03.10 2015 –≤ 17:00
–Т –і–Њ–њ—К–ї–љ–µ–љ–Є–µ:
–Ю—В –£–Є–Ї–Є–њ–µ–і–Є—П:
–Р—В–Њ–Љ–µ–љ —А–∞–і–Є—Г—Б (calc) --70 (67) pm
–Ъ–Њ–µ—В–Њ —Й–µ —А–µ—З–µ 0,07 –љ–∞–љ–Њ–Љ–µ—В—А–∞, –∞ –љ–µ –Ї–∞–Ї—В–Њ –µ –≤ —В–∞–±–ї–Є—Ж–∞—В–∞, –њ–Њ-–≥–Њ—А–µ –≤ —В–µ–Ї—Б—В–∞.
–Я–Њ—Б–ї–µ–і–љ–Є –Ї–Њ–Љ–µ–љ—В–∞—А–Є
dolivo
–Ч–µ–Љ–љ–∞—В–∞ —П–±—К–ї–Ї–∞: —Б—В–∞—А–∞ –Ї—Г–ї—В—Г—А–∞ –Ј–∞ –љ–Њ–≤–Є—В–µ –Ї–ї–Є–Љ–∞—В–Є—З–љ–Є –≤—А–µ–Љ–µ–љ–∞
dolivo
–Ч–µ–Љ—П—В–∞ –њ–Њ—В—К–Љ–љ—П–≤–∞. –Ъ–∞–Ї–≤–Њ –Њ–Ј–љ–∞—З–∞–≤–∞ —В–∞–Ј–Є —В—А–µ–≤–Њ–ґ–љ–∞ –Ї–ї–Є–Љ–∞—В–Є—З–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ј–∞ –±—К–і–µ—Й–µ—В–Њ?
Nikor
–Э–∞ 30 —Б–µ–њ—В–µ–Љ–≤—А–Є 1928 –µ –Њ—В–Ї—А–Є—В –њ–µ–љ–Є—Ж–Є–ї–Є–љ—К—В
–Я—А–Њ—Б—В –І–Њ–≤–µ–Ї
–Э–Њ–≤–Њ –Њ–±—П—Б–љ–µ–љ–Є–µ –Ј–∞ –≥–Є–≥–∞–љ—В—Б–Ї–Є—В–µ –µ–Ї—Б–њ–ї–Њ–і–Є—А–∞—Й–Є –Ї—А–∞—В–µ—А–Є –≤ –°–Є–±–Є—А
dolivo
–Ъ–ї–Є–Љ–∞—В–Є—З–љ–Є—П—В —Б–Ї–µ–њ—В–Є—Ж–Є–Ј—К–Љ вАУ –љ–∞–є-—Б–Ї—К–њ–∞—В–∞ –ї—К–ґ–∞ –љ–∞ –љ–∞—И–µ—В–Њ –≤—А–µ–Љ–µ