
Една от най-интензивно развиващите сe научни области в момента е епигенетиката. Тя изучава измененията на клетъчни или физиологични белези, които не се причиняват от промени в секвенцията на ДНК.
С други думи епигенетиката се занимава с изследването на фактори на околната среда, които включват или изключват гените и влияят на това как клетките ще разчитат гените. Тези промени могат да бъдат или да не бъдат наследяеми. Представката „епи-“ произлиза от гръцката επί-, която означава: над, извън, около.
Един от епигенетичните механизми, който влияе всеобхватно на човешката физиология е метилирането на ДНК. Той представлява прибавянето на метилови групи (CH3) към 2 от 4-те нуклеотидни бази в молекулата на ДНК (към цитозиновата-животни и адениновата-бактерии). Тази химична реакция променя функцията на ДНК, така че при по-ниски нива на метилиране гените са активни, а при по-високи – не.
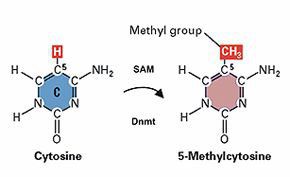 Прибавяне на метилова група към цитозин. Източник: premedhq.com
Прибавяне на метилова група към цитозин. Източник: premedhq.com
Едно любопитно изследване за влияние на метилирането на ДНК върху човешката физиология е проведено върху хора, изложени на глад преди раждането си през „Холандската гладна зима”, 1944 - 45. Този период на глад е резултат от наложената забрана от нацистка Германия за внос на храна в западните части на Нидерландия в края на Втората световна война. При тези хора гладуването в ранен период от развитието им е довело до повишен риск към синдром на Беквит-Уидеман (Beckwith-Wiedemann Syndrome). Заболяването се характеризира със свръхрастеж и рак.
В друго изследване е установено, че когато майката пуши по време на бременността, повлиява на родилното тегло на бебето чрез гореописания механизъм. Теглото на новороденото е по-ниско от нормалното.
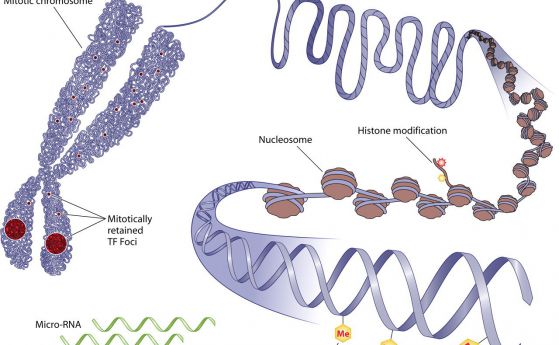
Епигенетичните промени имат ключови роли не само в ембрионалното развитие, но и в растежа и развитието при животните. Повечето сложни организми се развиват от специални репродуктивни клетки, каквито са яйцеклетките и сперматозоидите при човека. Когато две такива клетки се срещнат, те се сливат и се образува зигота. Зиготата расте, дели се, за да формира всеки тип клетка във възрастния организъм. Обаче за да се случи това, епигеномът трябва да бъде изчистен чрез процес, наречен „репрограмиране”.
Репрограмирането е важно, защото яйцеклетките и сперматозоидите се развиват от клетки, които са специализирали в синтез на определени протеини. С други думи, тяхната информация е отбелязана с епигенетични етикети. Преди новият организъм да порасне в здрав ембрион, тези етикети трябва да бъдат премахнати, за да може зиготата да образува всякакви видове клетки.
В определени периоди от развитието специализиран клетъчен механизъм изчиства генома и премахва неговите епигенетични етикети, за да върне клетките в генетично начално състояние.
При бозайниците около 1% от гените избягват епигенетичното репрограмиране чрез процес, наречен импринтинг. Той се извършва само при животните и цъфтящите растения. При геномният импринтинг в бозайниците потомството наследява само един работещ алел (вариант на гена). В зависимост от гена, един от двата алела, майчиния или бащиния, е дезактивиран или "заглушен". "Заглушаването" се извършва чрез прибавяне на метилова група по време на образуването на яйцеклетката или сперматозоида. Учените са разработили редица хипотези, за да обяснят защо се случва импринтирането, тъй като причината не е напълно изяснена. В една от тях, "хипотеза за генния конфликт", се изказва предложението, че механизма се появява като резултат от състезание между мъжките индивиди за майчините ресурси.
В някои видове повече от един мъжки може да стане баща на поколението от едно раждане. Например домашната котка може да се чифтоса повече от веднъж и котенцата в котилото да имат двама или повече бащи. Ако малките на един от бащите пораснат повече от останалите, неговото поколение ще има по-голям шанс да оцелее, за да станат възрастни и да предадат неговите гени по-нататък. В такъв случай е в интерес на бащините гени да създадат по-голямо поколение. По-големите котенца ще бъдат способни да се състезават за майчините ресурси за сметка на котенцата от другите бащи.
От друга страна, за майчините гени ще е по-добре, ако всички малки пораснат и се размножат. Майката ще нахрани и защити цялото си потомство по време на бременността си и след това. Тя трябва да е способна да разпредели ресурсите си между няколко животни.
Този конфликт на интереси между бащините и майчините импринтирани гени предизвиква епигенетична битка между родителите – един вид дърпане на въже между родителите, тъй като бащиният импринтинг благоприятства образуването на по-голямо потомство, а майчиния - на по-малко.
Епигенетичната наследственост придава ново измерение на модерната картина на еволюцията. Геномът се променя бавно чрез случайни мутации и естествен отбор. Сменят се много поколения, докато дадена генетична черта стане често срещана в популацията. От друга страна епигеномът може да се променя бързо в отговор на сигнали от околната среда. Епигенетични промени могат да се получат и в много индивиди едновременно. Чрез епигенетична наследственост, част от преживяванията на родителите могат да се предадат на бъдещите поколения. В същото време епигеномът остава гъвкав, докато условията на околната среда продължават да се променят. Епигенетичната наследственост позволява на организма постоянно да регулира дейността на гените си, за да се приспособи към външните условия без да променя своя ДНК код.
Използвани източници:
Epigenetics, Schahram Akbarian, Emily Bernstein, Patrizia Casaccia, Fatemah Haghighi, Yasmin Hurd, Paul Kenny, Javier Gonzalez-Maeso, Eric J. Nestler, Scott J. Russo, Anne Schaefer, Li Shen
Epigenetics, Genenic science learning center, The University of Utah
DNA methylation mediates the effect of maternal smoking during pregnancy on birthweight of the offspring, Leanne K Kupers, Xiaojing Xu, Soesma A Jankipersadsing...
Persistent epigenetic differences associated with prenatal exposure to famine in humans, Bastiaan T. Heijmans, Elmar W. Tobi, Aryeh D. Stein, Hein Putter, Gerard J. Blauw, Ezra S. Susser, P. Eline Slagboom and L. H. Lumey
Post-weaning diet affects genomic imprinting at the insulin-like growth factor 2 (Igf2) locus, Robert A. Waterland, Juan-Ru Lin, Charlotte A. Smith and Randy L. Jirtle













Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари