
Някои редки заболявания привличат учените и не ги оставят на мира, а необичайното заболяване наречено прогресивна фибродисплазия осификанс (fibrodysplasia ossificans progressiva - FOP) е един от примерите за такова заболяване, пленило завинаги интереса на Арис Економидес (Aris Economides). "В момента, в който се докоснеш до него е абсолютно невъзможно да го забравиш", твърди функционалния генетик, който отговаря за програмата за скелетни заболявания към фармацевтичната компания Regeneron Pharmaceuticals в Таритаун, щата Ню Йорк. "Това заболяване е ужасяващо във възможно най-дълбокия смисъл на думата."
Няколко хиляди човека с FOP по света живеят в изтощителна несигурност: Някои от техните мускули и други меки тъкани периодично, но внезапно могат да се трансформират в нова костна тъкан, която завинаги да обездвижи тези части от телата им. Ставите им, например тези на лакатите и глезените може буквално да се вкаменят; челюстите им да блокират, а гръдния им кош да се фиксира в плътна маса, което би направило храненето и дори дишането ужасно мъчителни.
20 години след като за пръв път се натъкнал на заболяването, Економидес и колегите му докладват, че генетичната мутация характерна за 97% от хората с това заболяване може би предизвиква симптомите му по начин различен от това, което се е смятало до момента - посредством молекула, която до сега не е влизала в полезрението на учените-специалисти. И по чиста случайност, компанията Regeneron съхранява във фризерите си лечение насочено към тази конкретна молекула. Компанията тествала този потенциален терапевтичен агент, представляващ моноклонално антитяло, върху миши модел на FOP и за тяхна изненада - то довело до пълно преустановяване на растежа на ненужното ново костно вещество.
Дали антитялото би проработило и при хора все още не е ясно. Regeneron продължават тестовете на медикамента и от компанията се надяват да се достигне до клинично изпитване. Учените-специалисти по заболяването приветстват новото откритие. "Бях наистина изненадана, че дефектният ген се държи по този начин," разказва Айлийн Шоор (Eileen Shore) от университета в Пенсилвания, генетик и клетъчен и молекулярен биолог, която е участвала пряко в откриването на FOP гена още през 2006 г. "Всички, които познавам, на които разказах за откритието се изненадани."
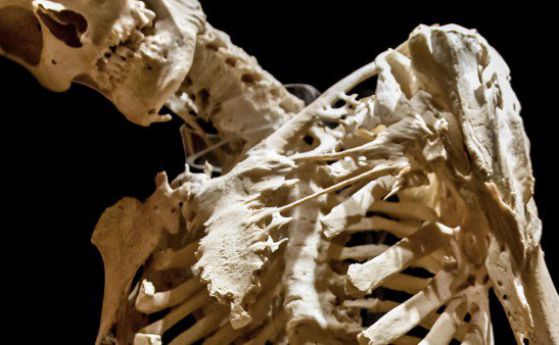
Економидес за пръв път разбира за заболяването FOP още през 1996 г., след като тъкмо бил приключил постдок програмата си към Regeneron, по това време млада биотехнологична компания насочила вниманието си основно към неврологични заболявания. Учените работещи там изучавали протеин при животни, когато осъзнали, че той може да спре натрупването на костно вещество, което пък ги довело и до FOP. Този протеин обаче не довел до разработване на медикамент. Междувременно Економидес се натъкнал на снимка на Хари Ийстлак (Harry Eastlac), пациент с FOP, който доброволно дарил скелета си, осеян с много допълнително слоеве новообразувана кост, след смъртта си на музея Mütter във Филаделфия, щата Пенсилвания. Економидес се срещнал с още хора страдащи от същото заболяване и техните лични драми останали с него, дори когато временно преустановил работата си над FOP.
 Тежки малформации при пациенти със заболяването, известно още като "Синдром на каменния човек" (Stone man syndrome)
Тежки малформации при пациенти със заболяването, известно още като "Синдром на каменния човек" (Stone man syndrome)
През 2006, учените открили генетичен дефект, който бил в основата на FOP: мутирала версия на гена ACVR1, който при пациентите страдащи от заболяването произвеждал свръхактивна форма на трансмембранен клетъчен рецептор по повърхността на клетките. Нормалната версия на рецептора се свързвала с естествения си молекулен партньор (лиганд), при което се изпращали сигнали в клетките, които подтиквали растежа на нова кост.
Економидес обаче останал озадачен - как точно дефектния ген може да предизвика такъв невероятен растеж на костно вещество при пациентите с FOP? През 2012 г., в Regeneron започнали активна работа по въпроса. Първият въпрос бил дали мутиралия ACVR1 рецептор при FOP се нуждае от лиганда си, за да предизвика свръхрастежа на костно вещество, или пък хроничната активност на рецептора може да предизвика сам по себе си растежа на нова кост. За да провери това, той и колегите му дали на мишки с FOP медикамент, който блокира взаимодействието лиганд-рецептор. Мишките останали цялостно здрави, което показало, че лиганда е необходим, за да се задейства свръхрастежа на кост.
Но при тази ситуация Економидес бил поставен пред дилема. Имало много потенциални лиганди за този специфичен рецептор и въпреки, че той можел да блокира всичките при мишки, той не можел да приложи това у човек без в процеса да се повлияят жизненоважни сигнални пътища, което може да предизвика множество сериозни странични ефекти. Той трябвало да открие нещо по-специфично. Кой от лигандите е виновникът? При експерименти с клетки, екипът учени с изненада открил, че семейство от лиганди, които те никога досега не смятали, че са свързани с FOP, наречени активини, активирали мутантната форма на ACVR1. Активините обикновено предотвратявали сигнализацията през нормалната форма на рецептора.
Друга следа дошла от работата на Фредерик Каплан (Frederick Kaplan) от Университета в Пенсилвания, ортопед-хирург и пионер в сферата на FOP, който изследвал заболяването от години и който помогнал много на екипа, който открил FOP гена. Изследванията на Каплан показвали, че FOP има възпалителен компонент - и, както се оказало, един от лигандите активини, означаван като активин А, участвал в процеса на възпаление.
Тези парчета допълнили пъзела на събитията. При здравите хора, активин А потиска нормалния ACVR1 рецептор, което поддържа костния растеж под контрол. Но при хората с FOP, както показват последните експерименти, активин А имал противоположен ефект върху мутантния рецептор, стумулирайки растежа на костта. Откритието е публувано тези дни в Science Translational Medicine
Парчетата на пъзела пасват чудесно и по още една причина: От отдавна е известно, че при пациентите с FOP е по вероятно да се появи растеж на кост при претърпяна травма, дори когато тя е малка например просто препъване. Активин А се произвежда след точно такива инциденти - протеина се секретира от имунни клетки при получаване на сигнал за наличие на травма. "Знаехме, че травмите са част от заболяването, но не знаехме точно какво се променя в тялото, за да се задейства растежа на костно вещества и появата на симптомите," разказва Пол Ю (says Paul Yu), който работи с FOP в болницата Brigham and Women’s Hospital в Бостън и е съ-автор в новата пибликация.
Остава да се установи дали антитялото, блокиращо активин А, с каквото разполагат Regeneron съхранено във фризерите си и вече са тествали върху мишки, ще подейства и при FOP пациенти. "Все още не знаем значението на това при хора," предпазлив е Каплан. В момента той провежда експерименти с клетки от пациенти с FOP и здрави контроли.
Източник: Science Magazine



















Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари
Johnny B Goode
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Gunteer
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Християнин
Това е кралят на тиквите: Тиквата му тежи над един един тон
dolivo
Сахара очаква 75% увеличение на валежите до 2100 г.