
Прочутият редактор на гени CRISPR може да се справя с мутации предивикващи болести. Това е показано лабораторно в клетъчни култури. Но как да се приложи методът на хора с генетични заболявания? Как ножиците на редактора да стигнат в тялото и срежат ДНК в точното място в тъканите, където това е необходимо? Това бе постигнато след еднократно инжектиране на CRISPR като лекарство в кръвта на хора с болест предизвикваща смъртоносна сърдечна и нервна болест – транстиретин амилоидоза (АТТР ). В провежданите клинични изпитания при трима от пациентите това довежда до почти пълно изключване на производството на токсичния белтък ТТР в техните черни дробове, и симптомите на заболяването се смегчават. (Транстиретиновата амилоидoза (АТТР) е рядко автозомно-доминантно заболяване, дължащо се на точкови мутации в гена за белтъка транстиретин (ТТР). Описано за първи път 1952 г. от португалския невролог Корино Андраде.ТТР представлява транспортен белтък за щитовидните хормони и ретинола.Той се синтезира в черния дроб. Мутациите дестабилизират молекулата на ТТР, субединиците се отделят и добиват нишковидна структура -амилоид.Първа среща на българските лекари с болен с АТТР е 2006 г.Общо досега са открити 89 семейства, а има клинични данни за над 100 заболели в регистъра.). Преди година CRISPR бе използванa за да се лекува сърповидната анемия и бета-таласемията. Взимат се кръвните клетки на болни, модифицират се ин витро чрез CRISPR и се инжектират отново в тялото. Инжектиране на лентивирус с CRISPR компоненти за поправяне на слепота също се изпробва. Трудно е с кръвопреливане да се изпратят терапевтични генетични инструкции до определен орган или тъкан. В това отношение черният дроб е удобен,
защото поема чужди частици от кръвта.Именно това е взето пред вид при използуване на метода за лекуване на амилоидозата.
За лекуване на амилоидозата CRISPR се прилага под формата на мРНК, подобно на Ковид-ваксините на Пфайзер и Модерна. Една мРНК молекула носи информация за ензима на CRISPR, както и за специфичен участък от ДНК – водеща РНК (gRNA), който определя прицела за ножиците на ензима Саs9,който да атакува както мутиралия така и здравия ген на TTР. мРНК е опакова в липидна обвивка, подбрана да влезе с лекота в черния дроб, докъдето стига по кръвен път. С успешния резултат фирмите Регенерон и Интелия Терапевтикс демонстрират с това лекарство - NTLA -2001 - възможностите на метода чрез кръвопреливане. В чернодробните клетки по информацията в мРНК се синтезира бактериалния белтък Cas.

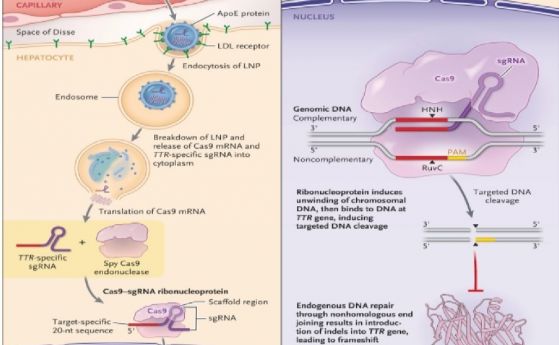
Panel A показва компонентите на NTLA-2001. Носителят на NTLA-2001 е липидна наночастица (LNP). LNP е йонизируем липид, комбиниран с фосфолипид, полиетилен гликол (мол. тегло 2000 Da), и холестерол, формулиран с воден буфер за интравенозно приложение. Активната компонента< на NTLA-2001 е оптимизирана мРНК, кодираща бактериалния ензим Streptococcus pyogenes (Spy) Cas9 (около 4400 нуклеотида) и водеща РНК (sgRNA) молекула (специфична за гена на човешкия ТТР). Това е „каргото“ на LNP, което се прилага интравенозно. В кръвта белтъка АроЕ опсонизира LNP и с това се улеснява поемането на NTLA-2001 директно и предимно в черния дроб. Panel B показва транспорта на NTLA-2001 LNP през капилярите чрез ендоцитоза и формиране на ендозоми в хепацитите на черния дроб. Там става „сваляне“ на опаковката – липидите и ендозомната мембрана, и активната РНК-компонента (ТТР-специфичната водеща sgРНК и мРНК, кодираща SpyCas9) се освобождава в цитоплазмата. мРНК на Cas9 минава през рибозомите и се транслира в ендонуклеазния ензим Cas9 . TТР-специфичната sgRNA взаимодейства с ендонуклеазата SpyCas9, образува рибонуклеотиден комплекс, който носи 20 нуклеотида специфични за прицелване в TTR- гена, и прониква в клетъчното ядро. Panel C Рибонуклеотидният комплексразпознава протоспейсъра (PAM) в ДНК на TTР гена, а 20-те нуклеотида в 5'- края на sgРНК намират точното място върху гена и позволява на CRISPR-Cas9 комплекса да развинти двойната спирала и да разреже прецизно ДНК в гена ТТР. ДНК- поправящите механизми зашиват скъсаното място, но това внася инсерции или делеции (indels). Наличието на indel може да доведе до намаляване на нивата на мРНК в целевия ген поради нонсенс или мис-сенс мутации. Те намаляват количеството на пълноценни мРНК, с краен резултат намалено нива на белтъка ТТР (както на мутантния така и на немутиралия). Такива индел мутации, намаляват продукцията на белтъка и се наричат нокаут мутации.
Фиг и статията са от DOI: 10.1056/NEJMoa2107454, J.D. Gilmour et al. New England J. Med June 29, 2021 “CRISPR-Cas9 In Vivo Gene Editing for Transthyretin Amyloidosis'
В клиничното изпитание на NTLA -2001 участват 6 души с ТТР амилоидоза, на които са инжектирани различни дози РНК кодираща CRISPR.
След 28 дни трима от пациентите получили по-високата доза лекарство показват 80-90% спадане на нивото на ТТР. За сравнение , използуваното досега лекарство патисиран използва антисенс- РНК за да унищожи временно производството на TTR. То трябва редовно да се прилага, а не еднократно с максимално спадане на ТТР нивото 80%.
Симптомите на заболяването започват да изчезват след месеци, за щастие без поява на съществени странични ефекти. По принцип ензимната ножица на CRISPR може да скъса на грешно място ДНК в черния дроб или другаде и дапредизвика рак или други проблеми. Засега не са установени подобни грешки. Липидната обвивка е по-удобна за ползуване от вирусните вектори(носители), носещи генетични инструкции. Доставената с липиди РНК изчезва (деградира се ) след като свършва редакционната си работа – намира точното място в генома на ТТР, скъсва ДНК там, след което клетъчната машинария поправя това скъсване. Но при поправката на скъсаната ДНК генът се разваля и престава да работи и нивото на ТТР пада (иначе казано генът е нокаутиран), а това води до положителен ефект от приложеното лечение.Това изследване отваря пътя за справяне с други чернодробни заболявания чрез метода CRISPR или чрез нокаутиране на гена, или, което е по-сложно, да го променят с помощта на ДНК образец.Така черният дроб може да бъде превърнат в фабрика за производство на ензим, необходим другаде из тялото. Дженифър Даудна (Jennifer Doudna) една от отривателките на CRISPR техниката, е съосновател на компанията Интелия, която с компанията Регенерон извършват клиничните изпитания на техния РНК продукт NTLA-2001. Тя казва,че това е съществена <стъпка към инактивиране, поправка, и замяна на всеки ген, който предизвиква болест някъде из тялото.
Използувана литература: J.D. Gilmour et al. New England J. Med June 29, 2021 “CRISPR-Cas9 In Vivo Gene Editing for Transthyretin Amyloidosis' DOI: 10.1056/NEJMoa2107454 и J. Kaiser Science 02 Jul 2021:Vol. 373, Issue 6550, pp. 16 DOI: 10.1126/science.373.6550.16
Авторът Константин Чипев е молекулярен и клетъчен биолог от Университета Стони Брук в Ню Йорк.
Още по темата
Животът
Ще унищожат ли биотехнологиите Homo sapiens?
Животът
Нови средства за онаследяване на епигенома (видео)

Животът
Генетичната ножица CRISPR-Cas9 - методът за промяна на кода на живота, удостоен с Нобелова награда

















Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари
"Ад" на Данте описва удар на астероид 500 години преди съвременната наука
10-годишно момиче открива рядък мексикански аксолотъл. Какво знаем за тези животни
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване