
Изследователи от Дрезден и Кеймбридж са идентифицирали клетъчен тип, който регулира регенерацията на черния дроб с докосване.
От времето на Аристотел е известно, че човешкият черен дроб има най-голям регенеративен капацитет от всеки друг орган в организма, като може да се възстанови дори при 70% ампутация, което позволява трансплантация от живи донори. Въпреки че черният дроб се регенерира напълно след увреждане, механизмите, които регулират как да се активира или спре процесът и кога регенерацията се прекратява, все още са неизвестни.
Изследователи от Института за молекулярна клетъчна биология и генетика на Макс Планк (MPI-CBG) в Дрезден (Германия), от Института Гърдън (Кеймбридж, Великобритания) и от Университета в Кеймбридж (департамент по биохимия) сега са установили, че регулаторният тип клетки - мезенхимните клетки - може да активира или спре регенерацията на черния дроб. Мезенхимните клетки го правят според броя на контактите, които установяват с регенериращите клетки (епителните клетки). Това проучване показва, че грешките в процеса на регенерация, които могат да доведат до рак или хронични чернодробни заболявания, са причинени от грешен брой контакти между двете популации. Работата е описана в статия, публикувана в списание Cell: Stem Cell.
Молекулярните механизми, чрез които зрелите чернодробни клетки предизвикват регенеративния отговор, остават до голяма степен неизвестни. Приблизително 29 милиона души в Европа страдат от хронично чернодробно заболяване като цироза или рак на черния дроб. Те са основна причина за заболеваемост и смъртност, като чернодробните заболявания представляват приблизително два милиона смъртни случая годишно в световен мащаб.
Понастоящем няма лечение и чернодробните трансплантации са единственото лечение за чернодробна недостатъчност. Затова учените проучват нови възможности за това как да се задейства регенеративната способност на черния дроб като алтернативно средство за възстановяване на функцията на черния дроб.
Разработване на мини черен дроб
Изследователи от Института по молекулярна клетъчна биология и генетика „Макс Планк“ в Дрезден заедно с колеги от Университета в Кеймбридж „Гърдън“ изучават биологичните принципи на регенерацията на черния дроб при възрастни. През 2013 г. Меритксел Хатч (Meritxell Huch), заедно с проф. Ханс Клевърс (Hans Clevers), разработват първите чернодробни органоиди - миниатюрни чернодробни тъкани, генерирани от чернодробни клетки на мишка в лабораторен съд.
Изследователите дори успешно трансплантират органоида в мишка, където той успява да изпълнява функциите на черен дроб. През 2015 г. успешно пренасят тази чернодробна органоидна технология за отглеждане на човешки черен дроб в лабораторен съд от биопсии на човешки черен дроб, а през 2017 г. разработват подобна система от тумор на човешки черен дроб. Лабораторията на Хатч се намира в Института Гърдън Gurdon на Университета в Кеймбридж до 2019 г. и след това се премества в MPI-CBG.
Изненадващо, вълнуващо наблюдение
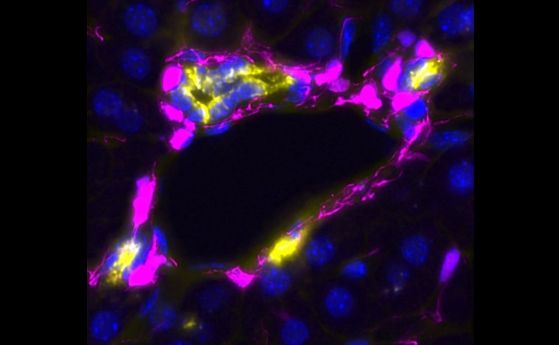
Две са основните функционални клетки на черния дроб - хепатоцитите, които изпълняват много от функциите на черния дроб, и дукталните клетки, които образуват мрежата от малки канали, доставящи жлъчката до червата. Те работят заедно с други поддържащи клетки, като кръвоносните съдове или мезенхимните клетки. За изграждане на чернодробни органоиди в началото изследователите са използвали само дуктални клетки на жлъчния канал. За да подобрят този модел и да го направят по-подобен на истинския черен дроб, докторантът Лусия Кордеро-Еспиноса (Lucía Cordero-Espinoza) и докторантът Анна Доубай (Anna Dowbaj) решават да построят по-сложен чернодробен органоид, който по-добре имитира клетъчните взаимодействия и архитектурата на чернодробната тъкан при възрастни. За това те добавят чернодробни мезенхими - вид регулаторни клетки на съединителната тъкан, които поддържат тръбната структура на жлъчния канал.
„Поставихме мезенхимните клетки до органоида, направен от дуктални клетки, в петриева чиния и видяхме, че те не се допират или свързват, както правят в естествената тъкан“, разказва Анна Доубай.
Изследователите се свързват с Флориан Холфелдер (Florian Hollfelder) от Университета в Кеймбридж, който познава метод, позволяващ комбинирането на клетките в малки гелове, които им позволяват да се срещнат и да установят контакт.
Анна Доубай продължава:
„Бяхме интригувани да видим как нашият нов и по-сложен органоид рекапитулира тъканната архитектура в лабораторен съд, затова решихме да проучим как се държат клетките и ги заснехме под микроскоп. За наша изненада видяхме напълно неочаквано поведение: тъканта (на органоида) се сви при допир с мезенхимните клетки, но нарасна при липса на контакти. Това парадоксално поведение бе поразително".
По-малко е повече и повече е по-малко
В здравия черен дроб има определен брой контакти между дукталните клетки и мезенхимните клетки, което казва на дукталните клетки да не правят повече от себе си и просто да останат такива, каквито са. След като тъканта претърпи увреждане, мезенхимните клетки намаляват броя на контактите си с дукталните клетки, така че те започват да се размножават, за да поправят увреждането. От своето наблюдение изследователите стигат до извода, че вместо абсолютният брой на двата типа клетки, броят на клетъчните контакти контролира колко клетки се произвеждат за възстановяване на увредената тъкан. Твърде много докосвания от мезенхимни клетки означава, че се произвеждат по-малко или никакви нови дуктални клетки, а по-малко докосвания означава, че се произвеждат повече клетки.
Меритксел Хатч, който ръководи проучването, заключава:
„За първи път успяхме да направим тези контакти видими и за първи път доказахме, че те съществуват. Успяхме да направим това поради нашите органоидни системи. Въпреки че проведохме експериментите си в лабораторен съд, извън живо тяло, ние смятаме, че същият процес протича и в живия организъм. Виждали сме това във фиксирани моменти от време по време на процеса на регенерация на увреждане, но досега не можехме да наблюдаваме това в жив организъм, тъй като липсва такава технология. Докато нашето проучване се фокусира върху дуктално-мезенхимните взаимодействия в черния дроб, можем да си представим, че подобни механизми се случват във всяка друга система, където броят на клетките се променя динамично, като белодробната или гръдната тъкан. Разбира се, в далечното бъдеще, бихме искали да създадем чернодробен органоид с всички типове клетки. С такъв органоид ще може да се тестват лекарства и да се види дали те влияят не само върху регенериращите клетки, но и върху тяхната поддържаща среда. Но за това трябва да изчакаме, докато стане налична такава технология".
Справка: “Dynamic cell contacts between periportal mesenchyme and ductal epithelium act as a rheostat for liver cell proliferation” by Lucía Cordero-Espinoza, Anna M. Dowbaj, Timo N. Kohler, Bernhard Strauss, Olga Sarlidou, German Belenguer, Clare Pacini, Nuno P. Martins, Ross Dobie, John R. Wilson-Kanamori, Richard Butler, Nicole Prior, Palle Serup, Florian Jug, Neil C. Henderson, Florian Hollfelder and Meritxell Huch, 2 August 2021, Cell Stem Cell.
DOI: 10.1016/j.stem.2021.07.002
Източник: How To Trigger and Control Liver Regeneration, WELLCOME TRUST/ CANCER RESEARCH UK GURDON INSTITUTE




















Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари
Gunteer
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Християнин
Това е кралят на тиквите: Тиквата му тежи над един един тон
dolivo
Сахара очаква 75% увеличение на валежите до 2100 г.
dolivo
Земната ябълка: стара култура за новите климатични времена