

–ü—Ä–ĺ–ľ–Ķ–Ĺ–ł –≤ –Ē–Ě–ö-—Ä–Ķ–∂–Ķ—Č–ł—Ź –Ķ–Ĺ–∑–ł–ľ Cas9 –Ņ—Ä–į–≤—Ź—ā CRISPR –ľ–Ķ—ā–ĺ–ī–į –∑–į –≥–Ķ–Ĺ–Ĺ–ĺ —Ä–Ķ–ī–į–ļ—ā–ł—Ä–į–Ĺ–Ķ –ľ–Ĺ–ĺ–≥–ĺ –Ņ–ĺ-–Ņ—Ä–Ķ—Ü–ł–∑–Ķ–Ĺ.
–ö–Ķ–Ļ—ā –Ē–∂—É–Ĺ–≥ –Ņ–ĺ–ľ–Ĺ–ł –Ņ—ä—Ä–≤–ł—Ź –Ņ—ä—ā, –ļ–ĺ–≥–į—ā–ĺ –Ņ—Ä–ĺ–Ī–≤–į–Ľ –ľ–Ķ—ā–ĺ–ī–į CRISPR. –í –ļ—Ä–į—Ź –Ĺ–į 2012 –≥., –Ņ–į—ā–ĺ–Ľ–ĺ–≥—ä—ā –ĺ—ā Massachusetts General Hospital –≤ –Ď–ĺ—Ā—ā—ä–Ĺ —Ā–≥–Ľ–ĺ–Ī–ł–Ľ –ļ–ĺ–ľ–Ņ–ĺ–Ĺ–Ķ–Ĺ—ā–ł—ā–Ķ –Ĺ–į –Ĺ–ĺ–≤–į—ā–į —ā–Ķ—Ö–Ĺ–ĺ–Ľ–ĺ–≥–ł—Ź –∑–į –≥–Ķ–Ĺ–Ĺ–ĺ —Ä–Ķ–ī–į–ļ—ā–ł—Ä–į–Ĺ–Ķ –ł —Ā–ł –Ņ–ĺ–ł–≥—Ä–į–Ľ —Ā –Ē–Ě–ö-—ā–ĺ –Ĺ–į –Ķ–ľ–Ī—Ä–ł–ĺ–Ĺ –Ĺ–į —Ä–ł–Ī–į—ā–į –∑–Ķ–Ī—Ä–į (zebrafish - —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ķ–Ĺ –Ķ–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–į–Ľ–Ķ–Ĺ –ĺ–Ī–Ķ–ļ—ā). "–Ď–Ķ—ą–Ķ —ā–ĺ–Ľ–ļ–ĺ–≤–į –Ľ–Ķ—Ā–Ĺ–ĺ," —Ā–Ņ–ĺ–ī–Ķ–Ľ—Ź —ā–ĺ–Ļ. "–Ě–į–Ņ—Ä–į–≤–ĺ –ł–∑—É–ľ–ł—ā–Ķ–Ľ–Ĺ–ĺ."
CRISPR –ľ–Ķ—ā–ĺ–ī—ä—ā - —Ā—ä—Ā—ā–ĺ—Ź—Č —Ā–Ķ –ĺ—ā –≤–ł—Ā–ĺ–ļ–ĺ–Ķ—Ą–Ķ–ļ—ā–ł–≤–Ķ–Ĺ –Ĺ–į–Ī–ĺ—Ä –ĺ—ā –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ—Ź—Ä–Ĺ–ł "–Ĺ–ĺ–∂–ł—Ü–ł", –ļ–ĺ–Ļ—ā–ĺ –Ĺ–į—Ā–ļ–ĺ—Ä–ĺ –Ī–Ķ –ĺ—ā–Ľ–ł—á–Ķ–Ĺ –ļ–į—ā–ĺ –Ě–į—É—á–Ķ–Ĺ –Ņ—Ä–ĺ–Ī–ł–≤ –Ĺ–į 2015 –≥–ĺ–ī–ł–Ĺ–į - –ľ–ĺ–∂–Ķ –ī–į –Ķ –Ľ–Ķ—Ā–Ķ–Ĺ –∑–į —É–Ņ–ĺ—ā—Ä–Ķ–Ī–į, –Ĺ–ĺ —Ā—ä–≤—Ā–Ķ–ľ –Ĺ–Ķ –Ķ –Ņ–Ķ—Ä—Ą–Ķ–ļ—ā–Ķ–Ĺ. –Ē–∂—É–Ĺ–≥ –ł –ļ–ĺ–Ľ–Ķ–≥–ł—ā–Ķ –ľ—É —Ā–ļ–ĺ—Ä–ĺ —É—Ā—ā–į–Ĺ–ĺ–≤–ł–Ľ–ł, —á–Ķ —ā–Ķ–∑–ł "–Ĺ–ĺ–∂–ł—Ü–ł" –ľ–ĺ–≥–į—ā –ī–į —Ä–Ķ–∂–į—ā –Ņ–ĺ–≤–Ķ—á–Ķ –ĺ—ā –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—ā–ĺ, –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ļ–ļ–ł –Ē–Ě–ö –Ĺ–į –Ĺ–Ķ–ĺ—á–į–ļ–≤–į–Ĺ–ł –ł –Ĺ–Ķ–∂–Ķ–Ľ–į–Ĺ–ł –ľ–Ķ—Ā—ā–į. –ü—Ä–ł —Ä–į–Ĺ–Ĺ–ł—ā–Ķ –Ķ–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā, —É—á–Ķ–Ĺ–ł—ā–Ķ –ĺ—ā–ļ—Ä–ł–Ľ–ł, —á–Ķ —ā–Ķ–∑–ł —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –Ķ—Ą–Ķ–ļ—ā–ł –ľ–ĺ–≥–į—ā –ī–į –≤—ä–∑–Ĺ–ł–ļ–Ĺ–į—ā –Ĺ–į –Ĺ—Ź–ļ–ĺ–ł –ľ–Ķ—Ā—ā–į –≤ –Ē–Ě–ö —Ā –Ņ—Ä–ł–Ī–Ľ–ł–∑–ł—ā–Ķ–Ľ–Ĺ–ĺ —Ā—ä—Č–į—ā–į —á–Ķ—Ā—ā–ĺ—ā–į, –ļ–į–ļ—ā–ĺ –ł –Ĺ–į —Ü–Ķ–Ľ–Ķ–≤–ł—ā–Ķ —É—á–į—Ā—ā—ä—Ü–ł. –Ę–ĺ–≤–į –Ķ —Ā–Ķ—Ä–ł–ĺ–∑–Ķ–Ĺ –Ņ—Ä–ĺ–Ī–Ľ–Ķ–ľ, –į–ļ–ĺ –≤—ä–∑–Ĺ–į–ľ–Ķ—Ä—Ź–≤–į–ľ–Ķ –ī–į –Ņ—Ä–Ķ–≤—ä—Ä–Ĺ–Ķ–ľ CRISPR –≤ –ĺ—Ā–Ĺ–ĺ–≤–į –∑–į –Ī—ä–ī–Ķ—Č–ł —ā–Ķ—Ä–Ķ–Ņ–ł–ł –Ņ—Ä–ł —Ö–ĺ—Ä–į, –Ĺ–į–Ņ—Ä–ł–ľ–Ķ—Ä –Ņ–ĺ–Ņ—Ä–į–≤—Ź–Ĺ–Ķ—ā–ĺ –Ĺ–į –ī–Ķ—Ą–Ķ–ļ—ā–Ĺ–ł –≥–Ķ–Ĺ–ł, –ļ–ĺ–ł—ā–ĺ –Ņ—Ä–ł—á–ł–Ĺ—Ź–≤–į—ā –ľ—É—Ā–ļ—É–Ľ–Ĺ–į –ī–ł—Ā—ā—Ä–ĺ—Ą–ł—Ź –ł–Ľ–ł –Ĺ–į—Ā–Ľ–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–ĺ –∑–į–Ī–ĺ–Ľ—Ź–≤–į–Ĺ–Ķ –Ĺ–į —á–Ķ—Ä–Ĺ–ł—Ź –ī—Ä–ĺ–Ī. –ě—Ā–Ĺ–ĺ–≤–Ĺ–ĺ—ā–ĺ –Ņ—Ä–ł—ā–Ķ—Ā–Ĺ–Ķ–Ĺ–ł–Ķ –Ĺ–į —É—á–Ķ–Ĺ–ł—ā–Ķ –Ķ, —á–Ķ –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–Ķ—ā–ĺ –Ĺ–į –Ĺ–Ķ–∂–Ķ–Ľ–į–Ĺ –≥–Ķ–Ĺ –ľ–ĺ–∂–Ķ –ī–į –Ņ—Ä–Ķ–ī–ł–∑–≤–ł–ļ–į –Ĺ–Ķ–ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ —Ä–į—Ā—ā–Ķ–∂ –ł —Ä–į–ļ.
–°–Ķ–≥–į, –Ē–∂—É–Ĺ–≥ –ł –ļ–ĺ–Ľ–Ķ–≥–ł—ā–Ķ –ľ—É —Ā–į –ĺ—ā–ļ—Ä–ł–Ľ–ł –Ĺ–į—á–ł–Ĺ –ī–į –Ĺ–į–Ņ—Ä–į–≤—Ź—ā CRISPR –Ņ–ĺ-–Ņ—Ä–Ķ—Ü–ł–∑–Ķ–Ĺ. –ü—Ä–ł –Ĺ–į–Ļ-–Ĺ–ĺ–≤–ĺ—ā–ĺ —Ā–ł –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–Ķ, —ā–Ķ —Ā–į –ľ–ĺ–ī–ł—Ą–ł—Ü–ł—Ä–į–Ľ–ł —Ä–Ķ–∂–Ķ—Č–ł—Ź –Ķ–Ĺ–∑–ł–ľ, –∑–į –ī–į –Ņ–ĺ–Ĺ–ł–∂–į—ā —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł—ā–Ķ –Ķ—Ą–Ķ–ļ—ā–ł –Ĺ–į –Ņ—Ä–į–ļ—ā–ł–ļ–į –Ņ–ĺ–ī –Ĺ–ł–≤–ĺ—ā–ĺ –Ĺ–į –ī–Ķ—ā–Ķ–ļ—Ü–ł—Ź.
"–°–ľ—Ź—ā–į–ľ, —á–Ķ –ł–ľ–į –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ—Ā—ā —ā–ĺ–≤–į –ī–į –Ķ —Ā–Ķ—Ä–ł–ĺ–∑–Ķ–Ĺ –Ņ—Ä–ĺ–Ī–ł–≤," —Ā–ľ—Ź—ā–į –Ē–∂–ł–Ĺ-–°–ĺ –ö–ł–ľ (Jin-Soo Kim), –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ—Ź—Ä–Ķ–Ĺ –Ī–ł–ĺ–Ľ–ĺ–≥ –ļ—ä–ľ –Ě–į—Ü–ł–ĺ–Ĺ–į–Ľ–Ĺ–ł—Ź –£–Ĺ–ł–≤–Ķ—Ä—Ā–ł—ā–Ķ—ā –≤ –°–Ķ—É–Ľ, –ļ–ĺ–Ļ—ā–ĺ –Ĺ–Ķ –Ķ —É—á–į—Ā—ā–≤–į–Ľ –≤ –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–Ķ—ā–ĺ. –Ě–ĺ —Ā—ā—Ä–Ķ–ľ–Ķ–∂—ä—ā –∑–į –Ņ–ĺ–ī–ĺ–Ī—Ä—Ź–≤–į–Ĺ–Ķ –Ĺ–į CRISPR –Ķ–ī–≤–į –Ľ–ł —Č–Ķ –Ņ—Ä–ł–ļ–Ľ—é—á–ł —ā—É–ļ. "–Ě—Ź–ľ–į –ľ–Ķ–ī–ł–ļ–į–ľ–Ķ–Ĺ—ā–ł –Ī–Ķ–∑ —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –Ķ—Ą–Ķ–ļ—ā–ł," –ĺ—ā–Ī–Ķ–Ľ—Ź–∑–≤–į —ā–ĺ–Ļ. –Ď–į–∑–ł—Ä–į–Ĺ–ł—ā–Ķ –Ĺ–į CRISPR —ā–Ķ—Ä–į–Ņ–ł–ł –≤—Ā–Ķ –ĺ—Č–Ķ —Ā–į –ī–į–Ľ–Ķ—á –ĺ—ā —ā–Ķ—Ā—ā–≤–į–Ĺ–Ķ –≤—ä—Ä—Ö—É —Ö–ĺ—Ä–į –ł –Ĺ–ł–ļ–ĺ–Ļ –Ĺ–Ķ –∑–Ĺ–į–Ķ –ļ–į–ļ–≤–į —Ä–Ķ–į–Ľ–Ĺ–į –Ņ—Ä–Ķ—Ü–ł–∑–Ĺ–ĺ—Ā—ā —Č–Ķ –Ķ –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–į.
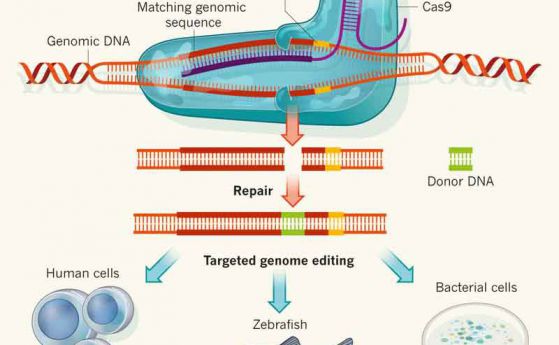
CRISPR —Ä–į–∑—á–ł—ā–į –Ĺ–į –Ē–Ě–ö-—Ä–Ķ–∂–Ķ—Č –Ķ–Ĺ–∑–ł–ľ –Ĺ–į—Ä–Ķ—á–Ķ–Ĺ Cas9, –Ņ—Ä–ł–ļ–į—á–Ķ–Ĺ –ļ—ä–ľ –ļ—ä—Ā–į –†–Ě–ö –Ņ–ĺ—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ–Ĺ–ĺ—Ā—ā, –ļ–ĺ—Ź—ā–ĺ –≥–ĺ –Ĺ–į—Ā–ĺ—á–≤–į –ļ—ä–ľ —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ–Ĺ —É—á–į—Ā—ā—ä–ļ –ĺ—ā –≥–Ķ–Ĺ–ĺ–ľ–į. –ö–ĺ–≥–į—ā–ĺ –†–Ě–ö-—ā–ĺ –Ĺ–į–ľ–Ķ—Ä–ł –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ľ–Ķ–Ĺ—ā–į—Ä–Ĺ–į - –ł–Ľ–ł –Ņ–ĺ—á—ā–ł –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ľ–Ķ–Ĺ—ā–į—Ä–Ĺ–į - –Ņ–ĺ—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ–Ĺ–ĺ—Ā—ā, Cas9 –ł–∑–≤—ä—Ä—ą–≤–į –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–Ķ –Ĺ–į –Ĺ—É–ļ–Ľ–Ķ–ĺ—ā–ł–ī–Ĺ–į—ā–į –≤–Ķ—Ä–ł–≥–į. –í–Ķ—á–Ķ –ł–ľ–į –Ĺ—Ź–ļ–ĺ–Ľ–ļ–ĺ –Ņ–ĺ–ī—Ö–ĺ–ī–į –∑–į –Ņ—Ä–Ķ–ī–ĺ—ā–≤—Ä–į—ā—Ź–≤–į–Ĺ–Ķ –Ĺ–į –Ĺ–Ķ–∂–Ķ–Ľ–į–Ĺ–ĺ—ā–ĺ –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–Ķ. –°–ļ—ä—Ā—Ź–≤–į–Ĺ–Ķ—ā–ĺ –Ĺ–į –ī—ä–Ľ–∂–ł–Ĺ–į—ā–į –Ĺ–į –≤–ĺ–ī–Ķ—Č–į—ā–į –†–Ě–ö —Ź –Ņ—Ä–į–≤–ł –Ņ–ĺ-—á—É–≤—Ā—ā–≤–ł—ā–Ķ–Ľ–Ĺ–į –Ĺ–į –Ĺ–Ķ—Ā—ä–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł—Ź, –Ĺ–ĺ —Ā—ä—Č–ĺ —ā–į–ļ–į –ľ–ĺ–∂–Ķ –ī–į –ī–ĺ–≤–Ķ–ī–Ķ –ī–ĺ —Ä–į–∑–Ņ–ĺ–∑–Ĺ–į–≤–į–Ĺ–Ķ –Ĺ–į –Ĺ–ĺ–≤–ł —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –ľ–ł—ą–Ķ–Ĺ–ł. –Ě—Ź–ļ–ĺ–ł –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–ł–ł —Ā–į –Ķ–ļ—Ā–Ņ–Ķ—Ä–ł–ľ–Ķ–Ĺ—ā–ł—Ä–į–Ľ–ł —Ā –≤–Ķ—Ä—Ā–ł—Ź –Ĺ–į Cas9, –ļ–ĺ—Ź—ā–ĺ –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į —Ā–į–ľ–ĺ –Ķ–ī–Ĺ–į—ā–į –≤–Ķ—Ä–ł–≥–į –Ĺ–į –Ē–Ě–ö –≤–ľ–Ķ—Ā—ā–ĺ –ł –ī–≤–Ķ—ā–Ķ. –Ę–ĺ–≤–į –ĺ–∑–Ĺ–į—á–į–≤–į, —á–Ķ –Ķ –Ĺ–Ķ–Ī—Ö–ĺ–ī–ł–ľ–ĺ –ī–≤–į Cas9 –Ķ–Ĺ–∑–ł–ľ–į –Ĺ–ĺ—Ā–Ķ—Č–ł —Ä–į–∑–Ľ–ł—á–Ĺ–ł –Ĺ–į—Ā–ĺ—á–≤–į—Č–ł –†–Ě–ö-–ł –ī–į —Ä–į–∑–Ņ–ĺ–∑–Ĺ–į—Ź—ā —Ā—ä–ĺ—ā–≤–Ķ—ā–Ĺ–į—ā–į —Ā–ł —Ü–Ķ–Ľ–Ķ–≤–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ–Ĺ–ĺ—Ā—ā, –∑–į –ī–į —Ā–Ķ –Ņ—Ä–Ķ—Ä–Ķ–∂–į—ā –ł –ī–≤–Ķ—ā–Ķ –≤–Ķ—Ä–ł–≥–ł - —ā–į–ļ–į –Ņ—Ä–ĺ—Ü–Ķ—Ā—ä—ā –Ĺ–į —Ā—ä–≤–Ņ–į–ī–Ķ–Ĺ–ł–Ķ –Ĺ–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ–Ĺ–ĺ—Ā—ā–ł—ā–Ķ –Ķ –ī–ĺ—Ā—ā–į –Ņ–ĺ-—Ā—ā—Ä–ł–ļ—ā–Ķ–Ĺ. –Ě–ĺ —É–ī–≤–ĺ—Ź–≤–į–Ĺ–Ķ—ā–ĺ –Ĺ–į –Ī—Ä–ĺ—Ź –Ĺ–į –≤–ĺ–ī–Ķ—Č–ł—ā–Ķ –†–Ě–ö-–ł —Ā—ä–∑–ī–į–≤–į –ł–∑–≤–Ķ—Ā—ā–Ĺ–ł –ĺ–≥—Ä–į–Ĺ–ł—á–Ķ–Ĺ–ł—Ź, –ļ–ĺ–ł—ā–ĺ –ľ–ĺ–≥–į—ā –ī–į –∑–į—ā—Ä—É–ī–Ĺ—Ź—ā –ī–ĺ—Ā—ā–į–≤—Ź–Ĺ–Ķ—ā–ĺ –Ĺ–į CRISPR-–Ī–į–∑–ł—Ä–į–Ĺ–ł —ā–Ķ—Ä–į–Ņ–ł–ł –≤ –ļ–Ľ–Ķ—ā–ļ–ł—ā–Ķ.
–í –Ĺ–ĺ–≤–ĺ—ā–ĺ –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–Ķ, –Ņ—É–Ī–Ľ–ł–ļ—É–≤–į–Ĺ–ĺ —ā–Ķ–∑–ł –ī–Ĺ–ł –≤ Nature, –Ē–∂—É–Ĺ–≥ –ł –ļ–ĺ–Ľ–Ķ–≥–ł—ā–Ķ –ľ—É —Ā–į –ł–∑–Ņ—Ä–ĺ–Ī–≤–į–Ľ–ł –ī—Ä—É–≥ –Ņ–ĺ–ī—Ö–ĺ–ī. –Ę–Ķ —Ā–į –ľ–ĺ–ī–ł—Ą–ł—Ü–ł—Ä–į–Ľ–ł¬†–Ķ–Ĺ–∑–ł–ľ–į Cas9, –∑–į –ī–į –Ņ—Ä–ĺ–ľ–Ķ–Ĺ—Ź—ā –Ĺ–į—á–ł–Ĺ–į, –Ņ–ĺ –ļ–ĺ–Ļ—ā–ĺ —ā–ĺ–Ļ –≤–∑–į–ł–ľ–ĺ–ī–Ķ–Ļ—Ā—ā–≤–į —Ā –Ē–Ě–ö. –ü—ä—Ä–≤–ĺ, —ā–Ķ –Ņ—Ä–ĺ–ľ–Ķ–Ĺ–ł–Ľ–ł –Ĺ—Ź–ļ–ĺ–ł –į–ľ–ł–Ĺ–ĺ–ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–Ĺ–ł –ĺ—Ā—ā–į—ā—ä—Ü–ł –Ņ–ĺ –Ņ–ĺ–≤—ä—Ä—Ö–Ĺ–ĺ—Ā—ā—ā–į –Ĺ–į –Ķ–Ĺ–∑–ł–ľ–į, –ĺ—ā –ļ–ĺ–ł—ā–ĺ —Ā–Ķ –ĺ—á–į–ļ–≤–į –ī–į –Ņ–ĺ–ī–Ņ–ĺ–ľ–į–≥–į—ā –∑–į —Ā–≤—ä—Ä–∑–≤–į–Ĺ–Ķ—ā–ĺ –Ĺ–į –≤–ĺ–ī–Ķ—Č–į—ā–į –†–Ě–ö —Ā—ä—Ā —Ā—ä–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–į—Č–į—ā–į –Ļ –≤–Ķ—Ä–ł–≥–į –≤ –Ē–Ě–ö. –ß–į—Ā—ā –ĺ—ā –ľ–ĺ–ī–ł—Ą–ł–ļ–į—Ü–ł–ł—ā–Ķ —Ā—ä–∑–ī–į–Ľ–ł –Ĺ–ĺ–≤ –≤–į—Ä–ł–į–Ĺ—ā –Ĺ–į Cas9, –ĺ–∑–Ĺ–į—á–į–≤–į–Ĺ –ļ–į—ā–ĺ Cas9-HF1, –ļ–ĺ–Ļ—ā–ĺ –ī–Ķ–ľ–ĺ–Ĺ—Ā—ā—Ä–ł—Ä–į –Ņ–ĺ-–≥–ĺ–Ľ—Ź–ľ–į —ā–ĺ—á–Ĺ–ĺ—Ā—ā –Ņ—Ä–ł –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–ł—Ź—ā–į, –ļ–ĺ–ł—ā–ĺ –ł–∑–≤—ä—Ä—ą–≤–į. –£—á–Ķ–Ĺ–ł—ā–Ķ –Ĺ–į–Ņ—Ä–į–≤–ł–Ľ–ł 7 —Ä–į–∑–Ľ–ł—á–Ĺ–ł –ľ–ĺ–ī–ł—Ą–ł—Ü–ł—Ä–į–Ĺ–ł –≤–į—Ä–ł–į–Ĺ—ā–į, –≤–ĺ–ī–Ķ–Ĺ–ł –ĺ—ā 7 —Ä–į–∑–Ľ–ł—á–Ĺ–ł –†–Ě–ö –≤–Ķ—Ä–ł–≥–ł, –∑–į –≤—Ā—Ź–ļ–į –ĺ—ā –ļ–ĺ–ł—ā–ĺ –Ī–ł–Ľ–ĺ –ł–∑–≤–Ķ—Ā—ā–Ĺ–ĺ, —á–Ķ –≥–Ķ–Ĺ–Ķ—Ä–ł—Ä–į —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –Ķ—Ą–Ķ–ļ—ā–ł —Ā –ĺ–Ī–ł–ļ–Ĺ–ĺ–≤–Ķ–Ĺ–ł—Ź Cas9. –£—á–Ķ–Ĺ–ł—ā–Ķ –ī–ĺ–ļ–Ľ–į–ī–≤–į—ā, —á–Ķ Cas9-HF1 –Ĺ–Ķ –Ņ–ĺ–ļ–į–∑–į–Ľ –ī–Ķ—ā–Ķ–ļ—ā–ł—Ä—É–Ķ–ľ–ł —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –Ķ—Ą–Ķ–ļ—ā–ł –≤ —ą–Ķ—Ā—ā –ĺ—ā —ā–Ķ–∑–ł —Ā–Ľ—É—á–į–ł - –ł —Ā–į–ľ–ĺ –Ĺ—Ź–ļ–ĺ–Ľ–ļ–ĺ —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–ł—Ź –Ņ—Ä–ł —Ā–Ķ–ī–ľ–ł—Ź —ā–Ķ—Ā—ā–≤–į–Ĺ –Ķ–Ĺ–∑–ł–ľ. –Ē–∂—É–Ĺ–≥ –ī–ĺ–Ī–į–≤—Ź, —á–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–≤–į–Ĺ–ł—ā–Ķ –Ņ–ĺ–≥—Ä–Ķ—ą–Ĺ–ł —Ā—Ä—Ź–∑–≤–į–Ĺ–ł—Ź –Ņ—Ä–ł –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł—Ź –ľ–ĺ–∂–Ķ –ī–į —Ā–Ķ –ī—ä–Ľ–∂–į—ā –Ĺ–į –≥—Ä–Ķ—ą–ļ–į –≤ —Ā–į–ľ–į—ā–į —Ā–Ķ–ļ–≤–Ķ–Ĺ—Ü–ł—Ź.
–ü–ĺ–ī–ĺ–Ī–Ĺ–ł —Ä–Ķ–∑—É–Ľ—ā–į—ā–ł –Ī—Ź—Ö–į –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ–ł –ł –ĺ—ā –Ķ–ī–ł–Ĺ –ĺ—ā –Ņ–ł–ĺ–Ĺ–Ķ—Ä–ł—ā–Ķ –≤ CRISPR –≥–Ķ–Ĺ–Ĺ–ĺ—ā–ĺ —Ä–Ķ–ī–į–ļ—ā–ł—Ä–į–Ĺ–Ķ, –§–Ķ–Ĺ–≥ –¶–ł–į–Ĺ–≥ (Feng Zhang) –ĺ—ā –•–į—Ä–≤–į—Ä–ī—Ā–ļ–ł—Ź —É–Ĺ–ł–≤–Ķ—Ä—Ā–ł—ā–Ķ—ā –ł Broad Institute –≤ –ö–Ķ–ľ–Ī—Ä–ł–ī–∂, —Č–į—ā–į –ú–į—Ā–į—á—É–∑–Ķ—ā—Ü, –Ņ—É–Ī–Ľ–ł–ļ—É–≤–į–Ĺ–ł –ľ–ł–Ĺ–į–Ľ–ł—Ź –ľ–Ķ—Ā–Ķ—Ü –≤ Science. –Ę–ĺ–∑–ł –Ķ–ļ–ł–Ņ —É—á–Ķ–Ĺ–ł –ľ–ĺ–ī–ł—Ą–ł—Ü–ł—Ä–į–Ľ–ł Cas9, –∑–į –ī–į –Ņ—Ä–ĺ–ľ–Ķ–Ĺ—Ź—ā –Ĺ–į—á–ł–Ĺ–į, –Ņ–ĺ –ļ–ĺ–Ļ—ā–ĺ —ā–ĺ–Ļ –ļ–ĺ–Ĺ—ā–į–ļ—ā—É–≤–į —Ā —Ä–į–∑–Ľ–ł—á–Ĺ–ł—ā–Ķ —á–į—Ā—ā–ł –Ĺ–į –Ē–Ě–ö –≤ –ļ–Ľ–Ķ—ā–ļ–į—ā–į. –Ę–ĺ–∑–ł –ľ–Ķ—ā–ĺ–ī —Ā—ä—Č–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ–Ĺ–ĺ –Ņ–ĺ–ī–ĺ–Ī—Ä–ł–Ľ —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ĺ–ĺ—Ā—ā—ā–į –Ĺ–į CRISPR. –í—Ā–Ķ –Ņ–į–ļ –Ķ —ā—Ä—É–ī–Ĺ–ĺ –ī–į —Ā—Ä–į–≤–Ĺ—Ź–≤–į–ľ–Ķ —ā–Ķ–∑–ł —Ä–Ķ–∑—É–Ľ—ā–į—ā–ł –ī–ł—Ä–Ķ–ļ—ā–Ĺ–ĺ —Ā —ā–Ķ–∑–ł –≤ –Ĺ–ĺ–≤–ĺ—ā–ĺ –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–Ķ, —ā—ä–Ļ –ļ–į—ā–ĺ —É—á–Ķ–Ĺ–ł—ā–Ķ —Ā–į –ł–∑–Ņ–ĺ–Ľ–∑–≤–į–Ľ–ł —Ä–į–∑–Ľ–ł—á–Ĺ–ł –ľ–Ķ—ā–ĺ–ī–ł –∑–į –ł–∑–ľ–Ķ—Ä–≤–į–Ĺ–Ķ –Ĺ–į —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł—ā–Ķ –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–ł—Ź.
–Ē–∂—É–Ĺ–≥ —ā–≤—ä—Ä–ī–ł, —á–Ķ –ł–∑–ľ–Ķ—Ä–≤–į–Ĺ–ł—Ź—ā–į –Ĺ–į –Ĺ–Ķ–≥–ĺ–≤–į—ā–į –≥—Ä—É–Ņ–į —Ā–į –ĺ–ļ–ĺ–Ľ–ĺ 10 –Ņ—ä—ā–ł –Ņ–ĺ-—á—É–≤—Ā—ā–≤–ł—ā–Ķ–Ľ–Ĺ–ł –ĺ—ā —ā–Ķ–∑–ł –ł–∑–Ņ–ĺ–Ľ–∑–≤–į–Ĺ–ł –Ņ—Ä–ł –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–Ķ—ā–ĺ –≤ Science. –ė –ī–≤–Ķ—ā–Ķ –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–ł—Ź —Ä–į–∑—á–ł—ā–į—ā –Ĺ–į –ľ–Ķ—ā–ĺ–ī–ł, –ļ–ĺ–ł—ā–ĺ –Ņ—Ä–ł–ļ–į—á–į—ā –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–Ĺ–ł –ľ–į—Ä–ļ–Ķ—Ä–ł –Ĺ–į –≤—Ā–ł—á–ļ–ł –ľ–Ķ—Ā—ā–į –≤ –≥–Ķ–Ĺ–ĺ–ľ–į, –ļ—ä–ī–Ķ—ā–ĺ —Ā–Ķ –Ķ –ĺ—Ā—ä—Č–Ķ—Ā—ā–≤–ł–Ľ–ĺ –ī–≤–ĺ–Ļ–Ĺ–ĺ–≤–Ķ—Ä–ł–∂–Ĺ–ĺ —Ā—Ä—Ź–∑–≤–į–Ĺ–Ķ, –Ņ—Ä–Ķ–ī–ł –ī–į —Ā–Ķ–ļ–≤–Ķ–Ĺ–ł—Ä–į—ā –ļ—ä—Ā–ł—ā–Ķ –ľ–į—Ä–ļ–ł—Ä–į–Ĺ–ł —Ā–Ķ–≥–ľ–Ķ–Ĺ—ā–ł, –∑–į –ī–į –Ņ—Ä–Ķ–Ī—Ä–ĺ—Ź—ā —Ā—Ä—Ź–∑–≤–į–Ĺ–ł—Ź—ā–į –≤ —Ä–į–∑–Ľ–ł—á–Ĺ–ł—ā–Ķ –≥–Ķ–Ĺ–ł. –Ē–∂—É–Ĺ–≥ –ł –ļ–ĺ–Ľ–Ķ–≥–ł—ā–Ķ –ľ—É —ā–≤—ä—Ä–ī—Ź—ā, —á–Ķ –ľ–ĺ–≥–į—ā –ī–į –∑–į—Ā–Ķ–ļ–į—ā —Ā—Ä—Ź–∑–≤–į–Ĺ–ł—Ź, –ļ–ĺ–ł—ā–ĺ —Ā–Ķ –ĺ—Ā—ä—Č–Ķ—Ā—ā–≤—Ź–≤–į—ā –≤ –Ņ–ĺ–Ĺ–Ķ 0,1% –ĺ—ā –≥–Ķ–Ĺ–ĺ–ľ–į. –¶–ł–į–Ĺ–≥ –Ņ—ä–ļ –ĺ—ā–Ī–Ķ–Ľ—Ź–∑–≤–į, —á–Ķ –ľ–Ķ—ā–ĺ–ī—ä—ā –≤ –Ĺ–Ķ–≥–ĺ–≤–ĺ—ā–ĺ –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–Ķ –Ķ —Ā –Ņ–ĺ—ā–≤—ä—Ä–ī–Ķ–Ĺ–į –Ķ—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā –ī–ĺ 0,3%, –Ĺ–ĺ —ā–ĺ–Ļ –ľ–ĺ–∂–Ķ –ī–į –Ķ –ī–ĺ—Ä–ł –ĺ—Č–Ķ –Ņ–ĺ-—á–≤—É—Ā—ā–≤–ł—ā–Ķ–Ľ–Ķ–Ĺ.
–Ē–į–Ľ–ł –ī–Ķ—ā–Ķ–ļ—ā–ł—Ä–į–Ĺ–Ķ—ā–ĺ –Ĺ–į —Ā–į–ľ–ĺ –Ĺ—Ź–ļ–ĺ–Ľ–ļ–ĺ –Ņ–ĺ–≥—Ä–Ķ—ą–Ĺ–ł —Ā—Ä—Ź–∑–≤–į–Ĺ–ł—Ź –Ĺ–į 1000 –ł–ľ–į –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ķ? –ź–Ī—Ā–ĺ–Ľ—é—ā–Ĺ–ĺ, —Ā–ľ—Ź—ā–į –Ē–∂—É–Ĺ–≥. "–ú–Ĺ–ĺ–≥–ĺ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ĺ–ł —Ā—ā—Ä–į—ā–Ķ–≥–ł–ł –Ņ—Ä–Ķ–ī–≤–ł–∂–ī–į—ā –Ņ–ĺ—ā–Ķ–Ĺ—Ü–ł–į–Ľ–Ĺ–ĺ—ā–ĺ –ľ–į–Ĺ–ł–Ņ—É–Ľ–ł—Ä–į–Ĺ–Ķ—ā–ĺ –Ĺ–į –ľ–ł–Ľ–ł–ĺ–Ĺ–ł, –ī–Ķ—Ā–Ķ—ā–ļ–ł –ľ–ł–Ľ–ł–ĺ–Ĺ–ł –ł –ī–ĺ—Ä–ł —Ā—ā–ĺ—ā–ł—Ü–ł –ľ–ł–Ľ–ł–ĺ–Ĺ–ł –ļ–Ľ–Ķ—ā–ļ–ł. –ó–į—ā–ĺ–≤–į 1 –Ĺ–į 1000 –∑–≤—É—á–ł –ī–ĺ—Ā—ā–į –ī–ĺ–Ī—Ä–Ķ, –Ĺ–ĺ —ā–į–∑–ł —Ā—ā–ĺ–Ļ–Ĺ–ĺ—Ā—ā –≤—Ā–Ķ –Ņ–į–ļ –ľ–ĺ–∂–Ķ –ī–į —Ā–Ķ –ĺ–ļ–į–∂–Ķ –Ņ—Ä–Ķ–ļ–į–Ľ–Ķ–Ĺ–ĺ –≤–ł—Ā–ĺ–ļ–į." –Ę–ĺ–Ļ —Ā–ľ—Ź—ā–į, —á–Ķ –ł–ľ–į –Ĺ—É–∂–ī–į –ĺ—ā —Ä–į–∑—Ä–į–Ī–ĺ—ā–≤–į–Ĺ–Ķ –Ĺ–į –Ņ–ĺ-–ī–ĺ–Ī—Ä–ł —ā–Ķ—Ā—ā–ĺ–≤–Ķ, –∑–į –ī–į —Ā–Ķ —Ā–≤–Ķ–ī–į—ā —ā–Ķ–∑–ł –Ņ–ĺ—ā–Ķ–Ĺ—Ü–ł–į–Ľ–Ĺ–ł –Ĺ–Ķ–∂–Ķ–Ľ–į–Ĺ–ł –Ķ—Ą–Ķ–ļ—ā–ł –ī–ĺ —á–Ķ—Ā—ā–ĺ—ā–į –ĺ—ā 0,01% –ł –ī–ĺ—Ä–ł –Ņ–ĺ-–ľ–į–Ľ–ļ–ĺ.
–Ē—Ä—É–≥–ł —Ā–į –Ņ–ĺ-–ľ–į–Ľ–ļ–ĺ –∑–į–≥—Ä–ł–∂–Ķ–Ĺ–ł –∑–į –Ņ–ĺ–≤–ł—ą–į–≤–į–Ĺ–Ķ—ā–ĺ –Ĺ–į —á—É–≤—Ā—ā–≤–ł—ā–Ķ–Ľ–Ĺ–ĺ—Ā—ā—ā–į –Ĺ–į —ā–Ķ—Ā—ā–ĺ–≤–Ķ—ā–Ķ. –Ę—ä–Ļ –ļ–į—ā–ĺ CRISPR –Ĺ–ł–ļ–ĺ–≥–į –Ĺ—Ź–ľ–į –ī–į –ī–ĺ—Ā—ā–ł–≥–Ĺ–Ķ –Ĺ–ł–≤–ĺ –Ĺ–į –Ĺ–ł–ļ–į–ļ–≤–ł —Ā—ā—Ä–į–Ĺ–ł—á–Ĺ–ł –Ķ—Ą–Ķ–ļ—ā–ł, –ļ–Ľ—é—á–ĺ–≤–ł—Ź—ā –≤—ä–Ņ—Ä–ĺ—Ā –∑–į –ī–į–ī–Ķ–Ĺ–į —ā–Ķ—Ä–į–Ņ–ł—Ź –Ĺ–Ķ –Ķ —ā–ĺ—á–Ĺ–ĺ –ļ–ĺ–Ľ–ļ–ĺ –Ĺ–Ķ–∂–Ķ–Ľ–į–Ĺ–ł –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–ł—Ź —Č–Ķ –ł–ľ–į, –į –ī–į–Ľ–ł —ā–ĺ–≤–į –Ĺ–į—Ä—É—ą–į–≤–į —Ą—É–Ĺ–ļ—Ü–ł–ł—ā–Ķ –Ĺ–į –∂–ł–∑–Ĺ–Ķ–Ĺ–ĺ–≤–į–∂–Ĺ–ł –≥–Ķ–Ĺ–ł, —Ā–ľ—Ź—ā–į –Ē–∂–ł–Ļ–Ĺ–≥-–ö—É–į–Ĺ –ô–Ķ (Jiing-Kuan Yee), –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ—Ź—Ä–Ķ–Ĺ –Ī–ł–ĺ–Ľ–ĺ–≥ –ĺ—ā –ł–∑—Ā–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ—Ā–ļ–ł—Ź —Ü–Ķ–Ĺ—ā—ä—Ä City of Hope –≤ –Ē—É–į—Ä—ā–Ķ, —Č–į—ā–į –ö–į–Ľ–ł—Ą–ĺ—Ä–Ĺ–ł—Ź. –í—Ā—Ź–ļ–ĺ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ĺ–ĺ –Ņ—Ä–ł–Ľ–ĺ–∂–Ķ–Ĺ–ł–Ķ —Č–Ķ –ł–∑–ł—Ā–ļ–≤–į —Ā–≤–ĺ–ł —Ā–ĺ–Ī—Ā—ā–≤–Ķ–Ĺ–ł –≤–Ĺ–ł–ľ–į—ā–Ķ–Ľ–Ĺ–ĺ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł—Ä–į–Ĺ–ł Cas9 –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–ł - –ł –ľ–ĺ–ī–ł—Ą–ł–ļ–į—Ü–ł–ł –ļ–į—ā–ĺ —ā–Ķ–∑–ł –ī–ĺ–ļ–Ľ–į–ī–≤–į–Ĺ–ł –≤ —ā–Ķ–∑–ł –ī–≤–Ķ –ł–∑—Ā–Ľ–Ķ–ī–≤–į–Ĺ–ł—Ź –ľ–ĺ–∂–Ķ –ī–į —Ā–Ķ –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–į—ā.
"–°–ľ—Ź—ā–į–ľ, —á–Ķ —Ā—ä–≤—Ā–Ķ–ľ —Ā–ļ–ĺ—Ä–ĺ –≤—Ā–ł—á–ļ–ł —Č–Ķ –∑–į–Ņ–ĺ—á–Ĺ–į—ā –ī–į –ł–∑–Ņ–ĺ–Ľ–∑–≤–į—ā —ā–Ķ–∑–ł –ľ–ĺ–ī–ł—Ą–ł—Ü–ł—Ä–į–Ĺ–ł Cas9 –Ķ–Ĺ–∑–ł–ľ–ł," —ā–≤—ä—Ä–ī–ł —ā–ĺ–Ļ. "–ü—Ä–ĺ–Ī–Ľ–Ķ–ľ—ä—ā —Ā—ä—Ā –Ņ–ĺ–≥—Ä–Ķ—ą–Ĺ–ł—ā–Ķ –Ņ—Ä–Ķ—Ä—Ź–∑–≤–į–Ĺ–ł—Ź –≤—Ā–Ķ –ĺ—Č–Ķ –ĺ—Ā—ā–į–≤–į, –Ĺ–ĺ –Ķ—Ą–Ķ–ļ—ā–ł—ā–Ķ –ľ—É —Č–Ķ –Ī—ä–ī–į—ā –∑–Ĺ–į—á–ł—ā–Ķ–Ľ–Ĺ–ĺ –Ņ–ĺ-–ĺ–≥—Ä–į–Ĺ–ł—á–Ķ–Ĺ–ł."
–ė–∑—ā–ĺ—á–Ĺ–ł–ļ: Science Magazine
–ě—Č–Ķ –Ņ–ĺ —ā–Ķ–ľ–į—ā–į
–Ė–ł–≤–ĺ—ā—ä—ā
–ó–į –Ņ—Ä—ä–≤ –Ņ—ä—ā –ł–∑–Ņ–ĺ–Ľ–∑–≤–į—Ö–į —ā–Ķ—Ö–Ĺ–ĺ–Ľ–ĺ–≥–ł—Ź –∑–į —Ä–Ķ–ī–į–ļ—ā–ł—Ä–į–Ĺ–Ķ –Ĺ–į –≥–Ķ–Ĺ–ł –Ĺ–į –∂–ł–≤ –Ī–ĺ–∑–į–Ļ–Ĺ–ł–ļ
–Ė–ł–≤–ĺ—ā—ä—ā
–ď–ĺ–Ľ–Ķ–ľ–ł—ā–Ķ –ĺ—ā–ļ—Ä–ł—ā–ł—Ź –≤ –ĺ–Ī–Ľ–į—Ā—ā—ā–į –Ĺ–į –Ī–ł–ĺ–Ľ–ĺ–≥–ł—Ź—ā–į –Ņ—Ä–Ķ–∑ 2015 –≥–ĺ–ī–ł–Ĺ–į
–ú–Ķ–ī–ł—Ü–ł–Ĺ–į
–ü—ä—Ä–≤–ĺ –Ņ—Ä–ĺ—É—á–≤–į–Ĺ–Ķ –∑–į –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ĺ–į —Ö–Ķ–ľ–ĺ—Ą–ł–Ľ–ł—Ź B —á—Ä–Ķ–∑ –≥–Ķ–Ĺ–Ĺ–ĺ —Ä–Ķ–ī–į–ļ—ā–ł—Ä–į–Ĺ–Ķ




















–ö–ĺ–ľ–Ķ–Ĺ—ā–į—Ä–ł
–ú–ĺ–Ľ—Ź, —Ä–Ķ–≥–ł—Ā—ā—Ä–ł—Ä–į–Ļ—ā–Ķ —Ā–Ķ –ĺ—ā T–£–ö!
–ź–ļ–ĺ –≤–Ķ—á–Ķ –ł–ľ–į—ā–Ķ —Ä–Ķ–≥–ł—Ā—ā—Ä–į—Ü–ł—Ź, –Ĺ–į—ā–ł—Ā–Ĺ–Ķ—ā–Ķ –Ę–£–ö!
–Ě—Ź–ľ–į –ļ–ĺ–ľ–Ķ–Ĺ—ā–į—Ä–ł –ļ—ä–ľ —ā–į–∑–ł –Ĺ–ĺ–≤–ł–Ĺ–į !
–ü–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł –ļ–ĺ–ľ–Ķ–Ĺ—ā–į—Ä–ł
Nikor
–Ě–į 30 —Ā–Ķ–Ņ—ā–Ķ–ľ–≤—Ä–ł 1928 –Ķ –ĺ—ā–ļ—Ä–ł—ā –Ņ–Ķ–Ĺ–ł—Ü–ł–Ľ–ł–Ĺ—ä—ā
–ü—Ä–ĺ—Ā—ā –ß–ĺ–≤–Ķ–ļ
–Ě–ĺ–≤–ĺ –ĺ–Ī—Ź—Ā–Ĺ–Ķ–Ĺ–ł–Ķ –∑–į –≥–ł–≥–į–Ĺ—ā—Ā–ļ–ł—ā–Ķ –Ķ–ļ—Ā–Ņ–Ľ–ĺ–ī–ł—Ä–į—Č–ł –ļ—Ä–į—ā–Ķ—Ä–ł –≤ –°–ł–Ī–ł—Ä
dolivo
–ö–Ľ–ł–ľ–į—ā–ł—á–Ĺ–ł—Ź—ā —Ā–ļ–Ķ–Ņ—ā–ł—Ü–ł–∑—ä–ľ ‚Äď –Ĺ–į–Ļ-—Ā–ļ—ä–Ņ–į—ā–į –Ľ—ä–∂–į –Ĺ–į –Ĺ–į—ą–Ķ—ā–ĺ –≤—Ä–Ķ–ľ–Ķ
helper68
–ė–∑–Ņ–ĺ–Ľ–∑–≤–į–Ĺ–Ķ—ā–ĺ –Ĺ–į —Ā–ľ–į—Ä—ā—Ą–ĺ–Ĺ –≤ —ā–ĺ–į–Ľ–Ķ—ā–Ĺ–į—ā–į –Ķ —Ā–≤—ä—Ä–∑–į–Ĺ–ĺ —Ā 46% –Ņ–ĺ-–≤–ł—Ā–ĺ–ļ —Ä–ł—Ā–ļ –ĺ—ā —Ö–Ķ–ľ–ĺ—Ä–ĺ–ł–ī–ł