
Хората, които консумират повече захар и други въглехидрати в продължение на дълъг период от време, имат повишен риск от развитие на автоимунни заболявания. Имунната система на тези пациенти атакува собствените клетки на организма, причинявайки например хронично възпалително заболяване на червата, заболяване на щитовидната жлеза и диабет тип 1.
Ново изследване на германски учени ще помогне да се идентифицират нови цели за лечение на редица подобни заболявания.
Молекулните механизми, лежащи в основата на автоимунните заболявания, са многопластови и сложни. В своето изследване учени от университета Юлий и Максимилиан във Вюрцбург, Германия, успяват да дешифрират нови подробности за тези процеси. Тяхната работа, публикувана в списание Cell Metabolism, подкрепя общоприетото схващане, че прекомерната консумация на глюкоза и други въглехидрати пряко допринася за развитието на патогенни функции в клетките на имунната система, и обратно, че нискокалоричната диета може да помогне за лечението имунни заболявания.
"Имунните клетки се нуждаят от големи количества захар под формата на глюкоза, за да изпълняват задачите си. С помощта на специализирани транспортери на клетъчната им мембрана, те могат да поемат глюкоза от околната среда", обяснява д-р Мартин Вет (Martin Väth), водещ автор на изследването.
Заедно с екипа си Мартин Вет от Института по системна имунология към Университета във Вюрцбург показва специалната роля на специфичен протеин за транспортиране на глюкоза, GLUT3, разположен в мембраната на много клетки, по-специално на имунните. Учените са установили, че в имунните Т-клетки този протеин изпълнява освен основната функция – пренос на глюкоза в клетката за производство на енергия – и допълнителни регулаторни функции.
Т-клетките или Т-лимфоцитите играят важна роля в придобития имунен отговор чрез разпознаване и унищожаване на клетки, които носят чужди антигени. Учените се фокусират върху специфична група Т-клетки, наскоро откритите Т-хелперни клетки тип 17, наричани още Th17 лимфоцити, които играят важна роля в регулирането на възпаленията и авто-възпалителните процеси. Основната задача на Т-хелперите е да разпознават заплахите и да засилят имунния отговор чрез активиране на други имунни клетки в тялото.
„Тези Th17 клетки експресират много GLUT3 протеин на клетъчната си повърхност", обяснява Вет.
Веднъж усвоена, глюкозата лесно се превръща в лимонена киселина в митохондриите, преди да се метаболизира в ацетил-коензим А (ацетил-КоА) в цитоплазмата. Ацетил-КоА участва в множество метаболитни процеси, включително биосинтеза на липиди.
Ацетил-КоА изпълнява допълнителни функции във възпалителните Th17 клетки, а също и допълнителни регулаторни функции.
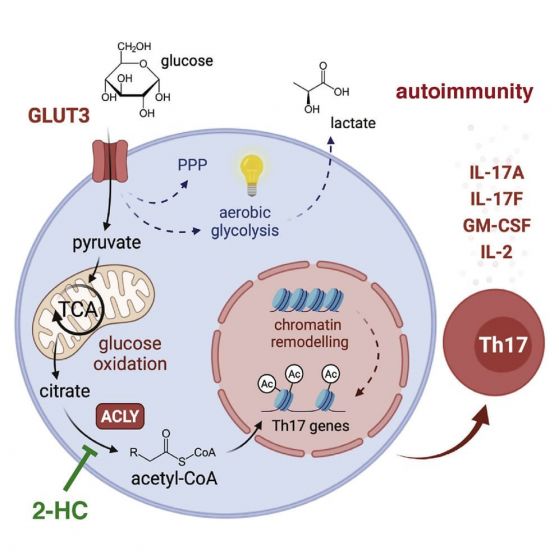 Описание на механизма, чрез който повишеният прием на глюкоза може да доведе до развитие на автоимунни възпалителни процеси поради активирането на специализирани гени в имунните Т клетки. Кредит: Hochrein S. M., et al, Cell Metabolism, 2022
Описание на механизма, чрез който повишеният прием на глюкоза може да доведе до развитие на автоимунни възпалителни процеси поради активирането на специализирани гени в имунните Т клетки. Кредит: Hochrein S. M., et al, Cell Metabolism, 2022
Д-р Вет и неговият екип показват, че този метаболитен междинен продукт може също да регулира експресионната активност на различни участъци на ДНК. По-специално, ацетил-КоА кара Th17 лимфоцитите да произвеждат повече провъзпалителни цитокини, сигнални молекули, които казват на други имунни клетки да започнат или да увеличат възпалителния процес. По този начин прекомерната консумация на глюкоза води до повишено натрупване на ацетил-КоА в Th17 лимфоцитите, което пряко влияе върху активността на провъзпалителните гени.
Според изследователите получените данни отварят пътя за разработване на нови подходи към целевата (таргетната) терапия на автоимунните заболявания. Например блокиране на GLUT3-зависим синтез на ацетил-КоА с хранителна биологично активна добавка, хидроксицитрат, използвана за лечение на затлъстяване. Тя може да смекчи патогенните функции на Th17 клетките и да отслаби възпалителните патологични процеси чрез потискане на прекомерните имунни и автоимунни отговори.
Така нареченото "метаболитно препрограмиране" на Т клетките отваря нови възможности за лечение на различни автоимунни заболявания, като хронични възпалителни заболявания на червата (болест на Крон и улцерозен колит) и щитовидната жлеза, както и захарен диабет тип 1 (в които инсулин-продуциращи клетки се унищожават), без да се намаляват защитните функции на имунните клетки.
Справка: Sophia M. Hochrein, Hao Wu, Miriam Eckstein, Laura Arrigoni, Josip S. Herman, Fabian Schumacher, Christian Gerecke, Mathias Rosenfeldt, Dominic Grün, Burkhard Kleuser, Georg Gasteiger, Wolfgang Kastenmüller, Bart Ghesquière, Jan Van den Bossche, E. Dale Abel, Martin Vaeth. The glucose transporter GLUT3 controls T helper 17 cell responses through glycolytic-epigenetic reprogramming. Cell Metabolism, 2022; DOI: 10.1016/j.cmet.2022.02.015
Източник: How sugar promotes inflammation
University of Würzburg
Още по темата

Животът
Дори умерените количества добавена захар удвояват производството на мазнини в тялото
Животът
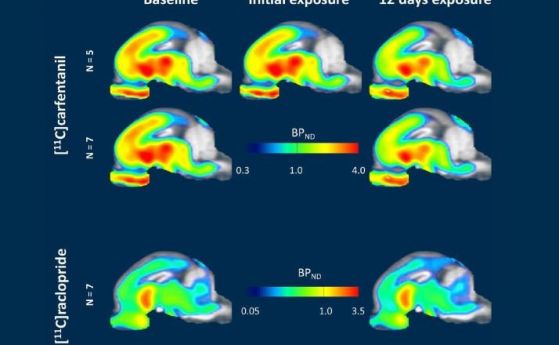
Захарта променя мозъчната химия според проучване върху малки прасета

Човекът
Остров Сардиния: голям брой столетници и много автоимунни болести














Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари
"Ад" на Данте описва удар на астероид 500 години преди съвременната наука
10-годишно момиче открива рядък мексикански аксолотъл. Какво знаем за тези животни
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване