
Генетичната информация се предава на поколенията чрез репликация на ДНК. Състоянието на генетична активност може да се предава на поколенията по не-генетичен път, т.е. - епигенетично.
В клетъчното ядро ДНК е опакована в белтък-ДНК комплекси, оформящи вериги от нуклеозоми, които са или в компактно състояние (хетерохроматин), или в разопаковано състояние (еухроматин).
Известно е, че хетерохроматиновите области могат да възстановят компактното си (неактивно) състояние и след митотични деления. Една нова публикация в списанието Cell показва, че при дрожди под влияние на външни фактори е възможно активната конформация също да се предава на следващите поколения.
За да се поддържа отворената активна структура на еухроматиновите области в клетъчното ядро, е необходимо присъствието на активатори (инициатори), които се свързват със специфични ДНК последователности, за да установят и поддържат хистоновите пост-транслационни модификации (ПТМ) и с това да се улесни транскрипцията на гените в еухроматина (вж. схемата по-нататък). Инициаторите привличат ко-активатори, например хистонови ацетилтрансферази, които ацетилират хистоните в близост до промоторни частъци ДНК. Лизин 16 на хистона Н4 е типична ПТМ (Н4К16ас), определяща еухроматина. В допълнение, в клетката се фосфорилира С-края на РНК полимераза-II (Ser5-P и Ser2-P), с което се привличат специфични метилтрансферази, метилиращи N-края на хистона H3 (H3K4 и H3K36) и така еухроматинът става компетентен да се транскрибира. След всеки репликационен цикъл, за да се възстанови активиращото ацетилиране Н4К16ас, отново се изисква присъствието на инициатор. Тоест: активираното хроматиново състояние не се предава епигенетично на следващото поколение. Такова е заключението на Reinberg и Vales от 2018. Именно това твърдение вече не е валидно (виж по-нататък в изложението).
В хетерохроматиновите области в клетъчното ядро гените са блокирани и не могат да работят. При дрождите тази инактивация се постига чрез отстраняване на ацетилните групи на хистона Н4. Деацетилирането се разпространява по съседните участъци и цялата хроматинова област се компактизира. Това състояние хистоновите деацетилази възпроизвеждат и след репликация. Може да кажем, че неактивното състояние на хроматина се предава епигенетично. При висшите еукариоти неактивният хроматин се характеризира с триметилираните лизини на хистона Н3 - Н3К27mе3 и Н3К9me3. Тези репресивни хистонови ПТМ са резултат от дейността на Поликомб-репресорния комплекс PRC2 и метилтрансферазата SUV39H1. Тези комплекси използуват процеса на „прочит“ (разпознаване на ПТМ), който активира ензимния модул на комплекса и прави „запис“ - метилиране на опашката на съседен хистон. Така се разпространява специфичното метилиране на хистоните по съседните нуклеозоми. Родителските репресивни ПТМ и присъствието на метилтрансферазата са достатъчни за възпроизвеждане на блокираното и неактивно геннo състояние в дъщерните клетки. При хетерохроматина неактивността се предава епигенетично през 100-тина митотични деления. При мейоза обаче репресивните ПТМ не оцеляват. Те се изтриват и не могат да се възпроизведат след клетъчното делене, освен в редки случаи.
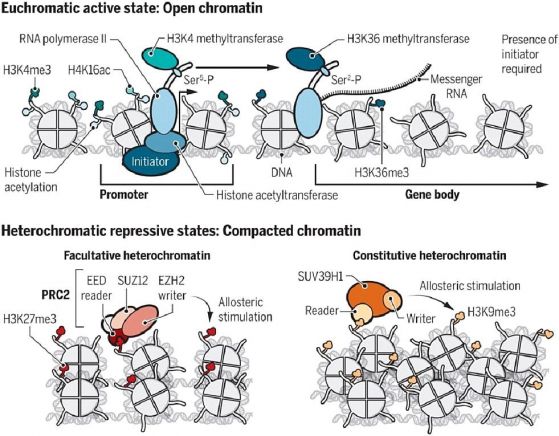
По Reinberg, D., and Vales, L.D. (2018). Chromatin domains rich in inheritance. Science 06 Jul 2018:Vol. 361, Issue 6397, pp. 33-34 Inheritance of repressive histone PTMs. DOI: https://doi.org/10.1126/science.aat7871
Неактивното състояние на хроматина може да се диктува и предава при репликация на ДНК и чрез метилирането нa цитозини, осъществявано с метилтрансферазите DNMT. При десетки хиляди митотичните деления метилираното състояние на нуклеотидите се възпроизвежда епигенетично в двете дъщерни двойни спирали. При мейоза обаче в почти всички случаи това не става.
Съществува и един чисто „белтъчен“ начин за предаване на епигенетична информация, определяща генната активност, и съответно състоянието на хроматина в клетката. Това става чрез приони. Те представляват специфично конформационно състояние на някои цитоплазмени белтъци. Прионната конформация е “заразна” и индуцира прехода на нормалните клетъчни форми на белтъка в прионни, при което „прионираните“ молекули образуват олигомерни агрегати. Такива са амилоидните плаки, намирани при болестта на Алцхаймер. Прионните агрегати могат да модулират генната активността в различни хроматинови области. При клетъчно деление те не се разреждат в дъщерните клетки и действат по не-Менделов начин. Така чрез прионите природата е измислила предаване на информация по чисто белтъчен път. Нещо повече, прионите оцеляват и се възстановяват количествено не само след 105 митотични деления, но и след мейотично делене, когато може да се говори за стабилен епигенетичен фенотип.
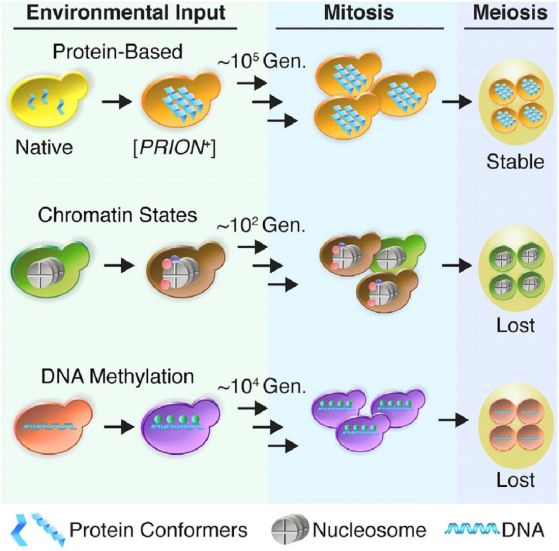
Трансгенерационна стабилност при различни видове епигенетично онаследяване. Различните цветове означават различни видове хроматин с активни или репресирани гени (в зависимост от промени в околната среда и митозата) и относителната им стабилност. Онаследяването при мейоза е в последната колона. То е налице само при участието на прионите.
Harvey, Z.H., Chen, Y., and Jarosz, D.F. (2018). Protein-based inheritance: epigenetics beyond the chromosome. Mol. Cell 69, 195–202. https://doi.org/10.1016/j.molcel.2017.10.030
За първи път в списанието Cell от 5 март 2020г. се съобщава за трансгенерационно епигенетично предаване и на активирано хроматиново състояние, осъществявано чрез приони.
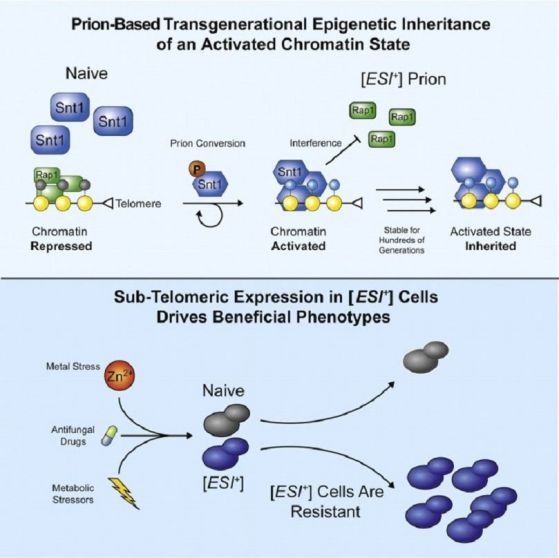
Zachary H.Harvey1Anupam K.Chakravarty1Raymond A.Futia2Daniel F.Jarosz. Cell Volume 180, Issue 5, 5 March 2020 A Prion Epigenetic Switch Establishes an Active Chromatin State, Pages 928-940. https://doi.org/10.1016/j.cell.2020.02.014
При дрожди се установява, че Snt1, част от репресорния хистон-деацетилазен комплекс Set3C (мейотично-специфичен репресор на ранни и средни гени за спорулация), може да действува като прион, който задвижва появата и унаследяването на генна активност през поколенията. Този прион, обозначен с [ESI+] за Експресирана Суб-теломерна Информация, е активиран (минал е в специфична прионова белтъчна конформация) чрез временното фосфорилиране на Snt1 предизвикано от стопиране на клетъчния цикъл. Влизайки в състава на Set3C комплекса (притежаващ и активиращи, и репресиращи функции), прионовото конформационно състояние на Snt1 (означено с шестоъгълници на схемата) променя активността си и накланя активността на комплекса Set3C в посока активиране. Тогава той привиква РНК полимераза II върху промотора, пречи на свързването на репресорния белтък Rap1, и така активира гените в дотогава репресираните суб-теломерни участъци. Това активно транскрипционно състояние придава широка устойчивост при стрес (с цинк Zn2+) и срещу фунгициди. Така прионите улесняват унаследяването на активно хроматиново състояние от полза за приспособяването към околната среда. Прионите Snt1 заместват ролята на четците и писарите в разпространението и унаследването на хроматиновото състояние при клетъчното делене. Това позволява реакцията на влиянието на околната среда със съпровождащата я генна активност да се запаметят епигенетично за идните поколения дори в отсъствие на външните фактори - своего рода унаследяване на придобити белези (в случая – резистентност на цинк и фунгициди). Прионите открехват една задна вратичка, през която да се промъкне духът на Ламарк. Засега такова явление не е регистирано при по-висшите организми. При тях в ембрионалното развитие всякакви епигенетични маркери в стволовите клетки се изчистват напълно.
Българската връзка: Преди 60 години на 1 април е основан Институтът по молекулярна биология на БАН с директор д-р Румен Цанев. Основна тематика скоро става изучаването на хроматина. Преди 50 години д-р Цанев създава своя молекулярен модел за клетъчна диференциация и определя хистоните като основни в епигенетичния код на клетката – гените са или блокирани, или неблокирани, а неблокираните могат да са репресирани или активни 1./. В годините след това сътрудниците на ИМБ изследват как хистоните осъществяват това епигенетично кодиране и механизма на унаследяване на епигенетичния код при репликация на ДНК 2./. Минават десетилетия и хистоновите варианти и модификации, и белязаната и определяна от тях генна активност на хроматина стават основна тема във водещите лаборатории по света. С основание може да се твърди, че ИМБ „Акад.Румен Цанев“ – БАН бе пионер в този вид изследвания. Честит юбилей!.
Източници:
1./ Tsanev R, Sendov B. J Theor Biol. Possible molecular mechanism for cell differentiation in multicellular organisms. 1971 Feb;30(2):337-93. https://doi.org/10.1016/0022-5193(71)90059-2.
2./ Russev, G., & Tsanev, R. (1979). Nonrandom segregation of histones during chromatin replication. European journal of biochemistry, 93(1), 123 – 128 DOI: https://doi.org/10.1111/j.1432-1033.1979.tb12801.x.
Авторът Константин Чипев е бивш сътрудник в Института по Молекулярна биология.
Още по темата

Животът
Може ли гладуването да ни направи по-умни?

Животът
Революционно откритие с българско участие за организацията на генома в клетъчното ядро

Животът
Парадоксът на ДНК на близнаците - НАСА провежда уникален експеримент (видео)












Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
1
11.04 2020 в 13:46
Последни коментари
"Ад" на Данте описва удар на астероид 500 години преди съвременната наука
10-годишно момиче открива рядък мексикански аксолотъл. Какво знаем за тези животни
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване
Астронавтите от Артемис 2 се завръщат на Земята (актуализирана)