
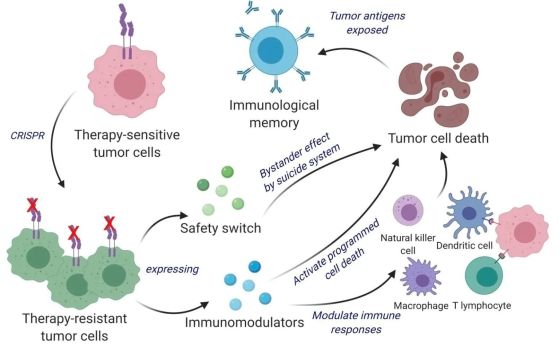
Ново изследване показва, че туморите са място за богата екосистема от бактерии и гъбички, които оказват влияние върху развитието на рака, което открива нови невероятни начини за борба с болестта.
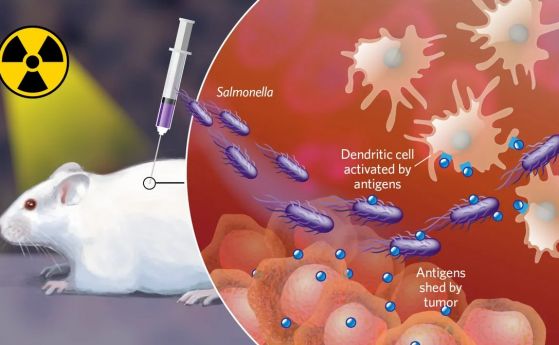
Бактериите салмонела обикновено се свързват с жестоки хранителни отравяния. Но през 2019 г. Ирит Балбул, 71-годишна канадка, доброволно изпива течност, съдържаща 1 милиард живи бактерии Salmonella typhimurium, като последна мярка срещу рака на панкреаса, който се е разпространил в други органи и й дава само месеци живот.
Бактериите са били генетично разработени така, че да предизвикат имунна атака срещу раковите клетки, като същевременно са по-малко токсични от обикновените салмонели за останалата част от организма. Балбул е първият човек в света, който ги изпробва заедно с химиотерапия, и туморите ѝ се свиват до едва 10 % от предишния си размер.
Може да звучи странно да се използват бактерии за лечение на рак, но методът е познат от края на XIX в., когато Уилям Коули (William Coley), хирург от Ню Йорк, започва да инжектира стрептококови бактерии в неоперативните тумори на някои от пациентите си, в резултат на което се наблюдава регресия, която той описва като "нищо друго освен чудо". Въпреки тези обещаващи резултати методът изпада в немилост. Повече от век по-късно обаче сме свидетели на завръщането на метода на Коули.
Микроорганизмите са естествено привлечени от туморите. Това е шанс за лечение
Вече е ясно, че много бактерии са естествено привлечени от туморите, които са убежище на богата микробна екосистема. Този туморен микробиом може да повлияе на развитието на рака и на реакцията му към лечението. По-ясното разбиране на тази система води до разработването на нови микробни лекарства, насочени срещу рака, някои от които вече са в процес на клинични изпитвания - включително и генно модифицираната салмонела. Тези микроби могат да проникнат дълбоко в места, които са трудно достъпни за съществуващите лечения, като например химиотерапията, и могат да бъдат снабдени с допълнителни оръжия за борба с рака чрез генно инженерство, предлагайки алтернативни начини за атака на туморите.
Повечето хора вече са запознати с чревния микробиом - сложната среда от бактерии, гъбички, вируси и други микроби, които обитават червата ни и влияят на здравето ни по безброй начини. Но идеята, че туморите също изобилстват от микроби, излезе на преден план едва през 2020 г., когато Илана Ливятан (Ilana Livyatan) от Научния институт "Вайцман" в Израел и нейните колеги анализират бактерии в повече от 1000 проби от човешки тумори.
Използвайки генетично секвениране, те идентифицират бактерии във всичките осем вида тумори, които изследват: гърда, мозък, бял дроб, кожа, кости, яйчници, панкреас и дебело черво.
"Това ни накара да повдигнем вежди и да си кажем: "Ей, какво правят те тук?", споделя Ливятан.
Средно откриват приблизително една бактериална клетка на всеки 150 туморни клетки, но някои видове тумори, като тези на дебелото черво и гърдата, обикновено съдържат повече бактерии от други. Още по-изненадващо е откритието, че всеки тип тумор има свой собствен микробен подпис.
Миналата година Ливятан и колегите ѝ пускат още една бомба: те откриват гъбички и в туморите, и то във всичките осем вида, които преди това са били положителни за бактерии. По същото време екип, ръководен от Илиян Илиев (Iliyan Iliev) от Университета Корнел в Ню Йорк, също е секвенирал ДНК на гъбички в редица тумори. Сред тях са гъбичките Candida - които по-често се свързват с вагиналната и оралната млечница - в ракови заболявания на стомаха, дебелото черво, главата и шията - макар че количествата са били незначителни: около една гъбична клетка на 10 000 туморни клетки.
"Това е нещо умопомрачително", разказва Илиев. "Изглежда, че нещо привлича гъбичките към някои тумори, защото когато разглеждаме туморна тъкан и съседна тъкан от един и същ пациент, виждаме, че гъбичните клетки са в преференциално изобилие в тумора".
 Д-р Илиян Илиев. Кредит: Weill Cornell Medicine
Д-р Илиян Илиев. Кредит: Weill Cornell Medicine
Кои микроорганизмите привличат туморите
Съществуват много причини, поради които микробите биха се привлекли в туморите, но става ясно, че тяхното присъствие може да повлияе на хода на рака и неговото лечение.
Бактериите, наречени Fusobacterium nucleatum, например, могат да стимулират развитието на рак на дебелото черво, да съпътстват разпространението му в други части на тялото и да отслабят реакцията му към химиотерапия. Тези бактерии живеят предимно в устата, но могат да навлязат в кръвообращението и след това да циркулират в дебелото черво. Там те могат да колонизират полипи - струпвания от клетки, които се образуват върху лигавицата на дебелото черво - и да ги превърнат в ракови. По подобен начин наличието на гъбички Malassezia globosa в туморите на гърдата, за които се предполага, че се придвижват дотам чрез каналите, свързващи кожата и гърдата, се свързва с по-лоша преживяемост.
От десетилетия знаем също, че някои вируси могат да предизвикат образуването на рак: например човешкият папиломен вирус (HPV) и вирусът на хепатит В (HBV), които се свързват съответно с рак на шийката на матката и на черния дроб. HPV вмъква своята ДНК в геномите на здравите клетки на маточната шийка и ги кара да растат неконтролируемо, превръщайки ги в ракови, а сега придобиваме по-ясна представа за механизмите, чрез които други микроби могат да повлияят на развитието на рака.
За щастие вече разполагаме с ваксини срещу HPV и HBV, които помагат за предотвратяване на свързаните с тях ракови заболявания. По същия начин може би ще бъде възможно да се разработят ваксини срещу бактерии, които стимулират развитието на тумори, обяснява Робърт Холт (Robert Holt) от Института за изследване на рака в Британска Колумбия, Канада. Те имат потенциала да потискат растежа на бактериите в съществуващите тумори, забавяйки развитието им и ги правят по-чувствителни към химиотерапия. Те биха могли дори да спрат образуването на тумори.
Холт и екипът му работят конкретно върху ваксина срещу бактерията F. nucleatum. Ваксината съдържа информационна (месинджър) РНК (мРНК), която е предназначена да инструктира организма да произвежда определени протеинови фрагменти, открити в тази бактерия. Идеята е да се обучи имунната система да разпознава и унищожава микроба.
На този етап ваксината все още се тества върху мишки, но Холт и колегите му се надяват един ден да я изпробват върху хора с положителен за F. nucleatum рак на дебелото черво, който е резистентен на конвенционалните лечения.
Една от стратегиите за справяне с рака е извеждането на "лошите" микроби от туморите, но друга може да бъде изпращането на "добри" микроби. Това е подходът, който Коули предприема, вдъхновен от прочетеното за мъж, чийто голям тумор на шията изчезва, след като развива инфекция със Streptococcus pyogenes на мястото, където хирургът му неуспешно се е опитал да изреже тумора.
Когато Коули инжектира живи S. pyogenes в туморите на 10 от пациентите си, при половината от тях туморите частично или напълно намаляват. Въпреки това той се затруднява да определи правилната доза и някои от по-късните му пациенти умират от лечението. В началото на XX век се появява лъчетерапията, която се смята за по-безопасна, и подходът на Коули остава на заден план.
Все още няма яснота как е действало лечението на Коули. Най-вероятно стрептококовите бактерии, които е инжектирал в туморите на пациентите си, са ги направили по-видими за имунната им система - разсъждава Ливятан. Въпреки че малки количества бактерии могат да се скрият в туморите поради механизмите на имунната защита на рака, инжектирането на големи дози от тях в туморите може да е достатъчно, за да се задейства алармата и имунната система да започне атака срещу раковите клетки, в които живеят бактериите, обяснява Ливятан.
"Свиването на тумора е поразително. Никой от нас не е виждал нещо подобно досега."
Изследванията на друга група в Научния институт "Вайцман", ръководена от Ярдена Самуелс, показват как бактериите на Коули са направили туморите по-видими за имунната система. Екипът открива, че протеинови фрагменти от бактерии, които колонизират меланомни ракови образувания на кожата, се експресират върху повърхността на раковите клетки. Те обозначават тумора като чужд за имунната система, така че тя да разбере: "Тук нещо не е наред" и да атакува раковите клетки, обяснява Ливятан.
Салмонелите, използвани за лечението на Балбул, са били генетично модифицирани, за да развият този механизъм още повече. Те са били модифицирани така, че да експресират протеин, наречен интерлевкин-2, който активира имунната система.
"Салмонелата отива директно в тумора и носи със себе си интерлевкин-2, така че не е изложен целият организъм на интерлевкин-2, а само туморът", обяснява Джеролд Батист (Gerald Batist), онкологът, който ръководи лечението на Балбул в Еврейската основна болница в Монреал. "Той създава имунна активност срещу тумора точно на мястото на тумора."
Балбул изпробва лечението наред със стандартната химиотерапия. Драматичното свиване на туморите ѝ показва много по-силна реакция, отколкото би се очаквало само при химиотерапия.
"Беше поразително - никой от нас не беше виждал подобно нещо преди", разказва Батист.
Нещо повече, бактериите не са разболели пациентката, добавя Батист.
"Идеята, че ще накараме някого да пие бактерии, наистина стресна инфекционистите от нашата комисия по етика, но това нямаше никакви странични ефекти."
След обещаващата реакция на Балбул към тези бактерии, Батист и колегите му започват фаза II на клинично изпитване през 2020 г. с участието на 20 души с метастатичен рак на панкреаса в четвърти стадий - считан за един от най-лошите от най-лошите видове рак. Всички участници в изпитването са били лекувани със стандартна химиотерапия плюс модифицираните салмонели. Резултатите, които са публикувани през януари, показват, че участниците са живели средно 24 месеца, което е повече от два пъти повече от типичната продължителност на преживяемост от 11 месеца само при стандартна химиотерапия. Салмонелата също не е разболяла доброволците.
Нови противоракови терапии
"Това не е чудодейно лекарство, но удвояването на преживяемостта е доста значимо, ако успеем да го потвърдим в по-големи проучвания", заявява Батист.
Основното предимство на този подход е, че бактериите са много по-евтини за производство, отколкото други имунотерапии за лечение на рак, като инхибитори на контролните точки, терапии с CAR Т-клетки и персонализирани ваксини, посочва Батист. Американската администрация по храните и лекарствата (FDA) наскоро дава на терапията със салмонела статут на ускорена, за да може тя да бъде достъпна възможно най-скоро, ако премине успешно бъдещите изпитвания. Миналата година проучване върху мишки показва, че бактериите, които се насочват към тумори, могат да бъдат контролирани с ултразвук, за да освобождават вещества, които се борят с рака, което предлага потенциален нов начин за прецизно насочване.
Компания в Швейцария, наречена T3 Pharma, също използва бактерии, за да се опита да засили имунната система срещу рака. Тя работи основно с бактерия, наречена Yersinia enterocolitica, която е контаминант на свинското месо и може да причини хранително отравяне, но е генетично модифицирана, за да се "намали нейната вирулентност", разказва Кристоф Каспер (Christoph Kasper), главен научен директор на фирмата.
Допълнителен бонус на Y. enterocolitica е, че има специални "наносиндроми" на повърхността си, които използва, за да инжектира протеини в клетките. T3 Pharma е разработила щам на Y. enterocolitica, който може да инжектира протеини в туморни клетки, за да ги накара да отделят сигнални молекули, които "действат като предупредителни сигнали, за да задействат имунната система в борбата с тумора", посочва Каспер.
Когато инжектира Y. enterocolitica в кръвта на мишки с меланом или други тумори, той избирателно се насочва към туморите и ги кара да изчезнат при до две трети от животните, без да има сериозни забележими странични ефекти. Компанията наскоро започна клинично изпитване на модифицираната Y. enterocolitica при хора с твърди тумори.
Компанията BioMed Valley Discoveries, базирана в Мисури, прилага различен подход, за да се насочи към нискокислородните джобове в туморите, които често са устойчиви на съществуващите лечения за рак. Тя инжектира спори на анаеробни бактерии Clostridium novyi, които са генетично модифицирани, за да бъдат по-малко токсични, директно в твърди тумори. Спорите покълват само в областите с ниско съдържание на кислород в туморите и с размножаването си предупреждават имунната система да започне да атакува тези области.
В първото изпитване върху хора, публикувано през 2021 г., бактериите са инжектирани директно в туморите на 24 души. Установено е, че те по същество втечняват вътрешността на тумора с ниско съдържание на кислород.
"Все още имаше пръстен от туморни клетки отвън, където туморите бяха добре оксигенирани и бактериите не можеха да се развиват, но в средата имаше само течност и газ, където клетките бяха унищожени", разказва Брент Крайдер (Brent Kreider), президент на BioMed Valley Discoveries.
Атакуване на туморите отвътре
Бактериите Clostridium сега се оценяват във второ клинично изпитване, този път в комбинация с инхибитора на контролната точка пембролизумаб (pembrolizumab) - по-известен като Keytruda - който може да се насочи към външните туморни клетки.
"Идеята е бактериите да се борят с тумора отвътре навън, а пембролизумабът да се бори с него отвън навътре", обяснява Крейдър.
Резултатите ще бъдат публикувани по-късно тази година, обявява Крейдър.
Бактериите обаче не са единствените микроби, на които се обръща внимание. Няколко вируси, които се борят с туморите, също са обект на изследване. Един от тях, наречен T-VEC, е одобрен от FDA през 2015 г. за лечение на меланом, който се е разпространил в други части на тялото. T-VEC използва щам на херпес симплекс вирус 1, който обикновено причинява афти, но е генетично модифициран, за да бъде по-малко вреден за здравите тъкани и да предизвиква имунна атака, когато се намира в тумори.
Това са някои от най-обещаващите истории, но в тази област има и разочарования. Изпитване на генетично модифицирани бактерии Listeria при хора с рак на белия дроб например бе прекратено през 2018 г., след като се оказа неефективно, а друго на генетично модифицирани Bifidobacterium при хора с различни видове тумори бе прекратено през 2021 г. по същата причина.
"Това е все още млада област и не е класически начин за подход към интервенцията при рак - инжектира се нещо живо, това не е като хапче - така че все още има много да се учи и може да бъде малко трудно", споделя Крейдър. "Но мисля, че има голяма надежда."
Що се отнася до Балбул, след като ѝ е било казано, че ѝ остават само месеци живот, тя в крайна сметка живее още над три години, докато наскоро умира на 74-годишна възраст.
"Ракът ѝ се върна и тя реши, че не иска по-нататъшно лечение", разказва Батист. "Но когато ѝ казах, че сме успели да започнем втора фаза на изпитване [на бактерията Salmonella], тя бе изключително развълнувана", разказва Батист.
Благодарение на смелостта, с която изпробва необичайното лечение, някога пренебрегнатият подход на Коули може би най-накрая ще намери място в съвременната медицина.
Справка:
Deborah Nejman et al.,The human tumor microbiome is composed of tumor type–specific intracellular bacteria. Science 3 68,973-980(2020). DOI:10.1126/science.aay9189
A pan-cancer mycobiome analysis reveals fungal involvement in gastrointestinal and lung tumors
Anders B. Dohlman, Jared Klug, Marissa Mesko, Steven M. Lipkin, Xiling Shen, Iliyan D. Iliev et al
DOI: https://doi.org/10.1016/j.cell.2022.09.015
Intratumoral Injection of Clostridium novyi-NT Spores in Patients with Treatment-refractory Advanced Solid Tumors
Filip Janku et al; Clin Cancer Res (2021) 27 (1): 96–106.
https://doi.org/10.1158/1078-0432.CCR-20-2065
Източник: Tumour-dwelling microbes: A startling new frontier in cancer treatment, New Scientist
Още по темата
Медицина
Революционна ваксина срещу рак едновременно убива и предотвратява мозъчни тумори
Медицина
Жена, диагностицирана 12 пъти с тумори, оцелява заради невиждана досега генетична мутация
Медицина
Инжектирането на салмонела помага на имунната система на мишките да убива тумори






















Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари
4I4ATA
Нов, скрит досега вход в пирамидата на Микерин е открит по аномалии при сканиране
YKoshev
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Johnny B Goode
Престижна награда от БАН спечели главният редактор на НаукаOFFNews
Gunteer
Престижна награда от БАН спечели главният редактор на НаукаOFFNews