

Нобеловият комитет на Каролинския институт (Karolinska Institutet) днес присъди Нобеловата награда за физиология и медицина за 2019 г. съвместно на Уилям Кейлин (William G. Kaelin Jr.), сър Питър Ратклиф (Sir Peter J. Ratcliffe) и Грег Семенса (Gregg L. Semenza) за техните открития върху клетъчната чувствителност и адаптивност към промяната в нивата на кислород.
Животните се нуждаят от кислород, за да превръщат храната в енергия. Фундаменталната важност на кислорода е известна от векове, но по какъв начин клетките се адаптират към промяната в нивата му, оставаше неясно.
Уилям Кейлин, сър Питър Ратклиф и Грег Семенса откриват как клетките усещат и се адаптират към променивото наличие на кислород.
Откритието на тазгодишните носители на наградата разкрива механизма на един от най-важните адаптационни процеси. Това помага да разберем как нивата на кислород влияята върху клетъчния метаболизъм и физиологичната функция. Откритията на тримата учени могат да бъдат използвани и при разработването на нови стратегии за борба с анемията, рака и много други заболявания.
Кислородът, О2, съставя около 1/5 от земната атмосфера. Кислородът е незаменим за човешкия живот - използва се от митохондриите, присъстващи във всяка животинска клетка, за да превръща храната в използваема енергия. Ото Варбург (Otto Warburg), носител на Нобеловата награда за физиология и медицина през 1931 г., разкрива, че този преход е ензимен процес.
С еволюцията се развиват механизми, които да осигурят достатъчно наличие на кислород в клетките и тъканите. Каротидното телце, прилежащо към големите каротидни артерии от двете страни на врата, съдържат специални клетки, които усещат нивата на кислород в кръвта. Нобеловият лауреат от 1938 г. Корней Ейман (Corneille Heymans) открива как при преминаването на кръвта през каротидното телце, промяната в парциалното налягане на кислорода и въглеродния диоксид, води до контрол на дишането чрез пряка връзка с мозъка.
В допълнение на бързата адаптация към ниските кислородните нива (хипоксия), контролирана от каротидното телце, съществуват и други фундаментални физиологични адаптации. Ключовият физиологичен отговор на хипоксията е повишаване на нивата на хормона еритропоетин (erythropoietin (EPO)), което води до повишено производство на червени кръвни клетки (еритропоеза). Важността на хормоналния контрол на еритропоезата е известна още от началото на 20-ти век, но досега оставаше неясно как този процес се самоконтролира чре кислорода.
Грег Семенса изучава гена за ЕРО и как се регулира от вариращите на нивата на кислород. Използвайки генно-модифицирани мишки, ученият открива, че специфични ДНК сегменти, разположени близо до гена за ЕРО, са свързни с отговора на хипоксията. Сър Питър Ратклиф също изучава кислородзависимата регулация на ЕРО гена и двата екипа откриват, че механизма на чувствителност към кислорода присъства във всички тъкани, не само в бъбречните клетки, където ЕРО се произвежда по принцип. Това са важни открития, показващи, че този механизъм е общ и функционира в много различни типове клетки.
Семенса иска да открие и клетъчните компоненти, улесняващи този отговор. В лабораторно отгледани клетки от черен дроб той открива комплекс, който се свръзва с идентифицираните ДНК сегменти, по кислородзависим начин. Той нарича този комплекс "фактор, поредизвикан от хипоксия" (hypoxia-inducible factor (HIF)). Опитите за извличане на HIF комплекса започват и през 1995 г. Семенса публикува някои от ключовите си открития, включително и идентификацията на гените, отговорни за HIF. Доказано е, че HIF се състои от два различни ДНК-свързващи протеина, т.нар. транскрипторни фактори, наречени HIF-1α и ARNT. Сега учените могат да започнат да разрешават загадката, като разберат кои допълнителни компоненти участват и как функционира целият механизъм.
Когато нивата на кислород са високи, в клетките се съдържа много малко HIF-1α. Когато нивата на кислород са ниски, количеството HIF-1α се повишава, така че да може да се свърже и така да регулира ЕРО гена, както и други гени със HIF-свързващи ДНК сегменти (Фигура 1.). Няколко екипа доказват, че HIF-1α, който по принцип бързо се разпада, е предпазен от разграждане в хипоксия. При нормални нива на кислорода, клетъча структура, наречена протеазома и също описана от нобелови лауреати, разгражда HIF-1α. При такива условия, малък пептид, убиквитин, се добавя към HIF-1α протеина. Убиквитина действа, като маркер за протеини, които трябва да бъдат разградени в протеазомата. Главният въпрос оставаше по какъв начин пептида се свързва с HIF-1α по кислородзависим начин.
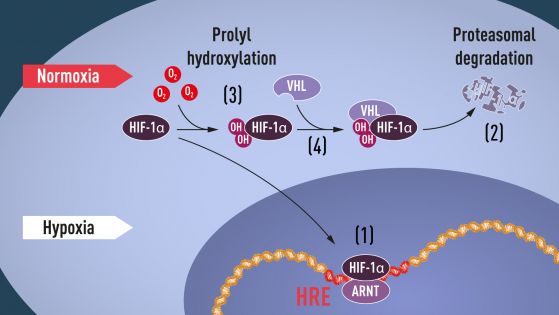 Фигура 1. Кредит: The Nobel Prize
Фигура 1. Кредит: The Nobel Prize
Отговорът идва от неочаквано място. Почти по същото време, когато Семенса и Ратклиф изучават регулацията на ЕПО гена, изследователя на рака Уилям Кейлин проучва наследствен синдром - болест на фон Хипел-Линдау (von Hippel-Lindau’s disease (VHL disease)). Това генетично заболяване води до драматично повишен риск от развитие на някои туморни заболявания при семейства, обременени с VHL мутации. Кейлин доказва, че генът за VHL кодира протеин, който предпазва от развитието на рак. Той открива и че туморните клетки, които не носят функционален VHL ген, проявяват ненормално високи нива на гени, регурирани от хипоксията. Но когато генът за VHL се въведе отново в клетката, нормалните нива се възстановяват. Това е важно доказателство, че VHL е свързан някак с контрола на отговора на хипоксията. Допълнителни доказателства идват и от други екипи, изучаващи VHL, които показват, че той е част от комплекс, свързващ протеини с убиквитин, за да бъдат разградени в протеазомата. Ратклиф и колегите му правят ключово откритие - демонстритат, че VHL може физически да взаимодейства с HIF-1α и е необходим за разграждането му при нормални нива на кислород. Това свързва пряко VHL с HIF-1α.
Много от въпросите получават отговор, но все още не е ясно как нивата на кислород регулират взаимодействието между VHL и HIF-1α. Изследванията се съсредоточават върху специфична част от HIF-1α протеина, необходима за разграждането, зависещо от VHL, и Кейлин и Ратклиф предполагат, че именно там е връзката с чувствителността към кислорода. През 2001 г., в две статии, публикувани едновременно, те показват, че при нормални нива на кислород, на две специфични позиции в HIF-1α се добавят хидроксилни групи (Фигура 1.). Тази промяна на протеина, наречена пролил хидроксилация, позволява на VHL да разпознае и да се свърже с HIF-1α и така се обяснява как нормалните нива на кислород контролират бързото разграждане на HIF-1α с помощта на кислородчувствителни ензими (т.нар. пролил хидроксилази). Доказва се и че ген-активиращата функцията на HIF-1α се регулира от кислородзависима хидроксилация. Така нобеловите лауреати обясняват и описват механизма на чувствителността към кислорода.
Благодарение на това откритие, сега се знае много повече за това как различните нива на кислород могат да регулират фундаментални физиологични процеси. Чувствителността към кислорода позволява на клетките да адаптират метаболизма си към ниски нива на кислород - например в мускулите при интензивни натоварвания. Други примери за адаптивни процеси, контролирани от чувствителността към кислорода са и създаването на нови кръвоносни съдове и производството на червени кръвни клетки. Имунната ни система и много други физиологични функции са контролирани от механизма на чувствителност към кислорода. Той е важен и при развитието на плода, за контрол на нормалното формиране на кръвоносните съдове и развитието на плацентата.
 Фигура 2. Кредит: The Nobel Prize
Фигура 2. Кредит: The Nobel Prize
Чувствителността към кислорода е важна и при голям брой заболявания (Фигура 2.). Например пациенти с хронична бъбречна недостатъчност често страдат от тежка анемия заради по-слаба генна експресия на ЕРО. Още повече, механизмът на кислородна регулация играе роля и при раковите заболявания. При туморните заболявания, той се използва да стимулира създаването на кръвоносни съдове и пренастройване на метаболизма за ефективно изчистване от туморните клетки. Интензивната работа на учените и на фармацевтичните компании са насочени към разработването на лекарства, които могат да лекуват различни заболявания чрез активирането или блокирането на механизма на кислородна чувствителност.
Източник: The Nobel Prize - Press release: The Nobel Prize in Physiology or Medicine 2019























Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари
"Ад" на Данте описва удар на астероид 500 години преди съвременната наука
10-годишно момиче открива рядък мексикански аксолотъл. Какво знаем за тези животни
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване
Хората с тъмни черти на характера са естествено склонни към лидерски роли, установява ново проучване