
Транс-генерационното епигенетично унаследяване е предаването на епигенетични маркери и модификации от поколение на поколение, без да се променя първичната структура на ДНК (т.е. последователността на нуклеотидите).
По този начин регулирането на гените чрез епигенетични механизми може да бъде унаследено; транскрипцията и произведените протеини могат да бъдат модулирани от унаследени епигенетични промени.До голяма степен е прието, че биологичното наследство се определя главно от унаследяването на геномната ДНК, но, макар и рядко, има и случаи на епигенетичнo унаследяване. Такива са широко документирани при бактериите, и някои безгръбначни животни. При бозайниците това е много рядко явление. Нарича се епимутация.
Епимутация: Наследствена промяна в активността на гените, която не е свързана с ДНК мутация, а по-скоро с придобиване или загуба на ДНК-метилиране или други наследствени модификации на хроматина. Пример за епимутация е абнормалното метилиране на CGI, което корелира с абнормални физиологични промени и неврологични, метаболитни и ракови заболявания, които се наблюдават и в следващи поколения.
Това означава, че епимутацията се унаследява. Дали тя е причината за дефектите не може да се каже, защото не е изключено да има генетични мутации, свързани с епимутацията.
В работата представено по-нататък се показва, че без странични генетични мутации , една изкуствено предизвикана епимутация води до а/ патологични дефекти и б/ се запазва в следващи поколения.
За да не се допусне подобно унаследяване на епигенетични промени организмите минават през две фази на епигенетично препрограмиране:
1. Изтриване на ДНК метилирането в целия геном (както и размяна на хистонови варианти и намаляване на хистоновите модификации в първичните зародишни клетки, прекурсори на гаметите.).
2. Това първо препрограмиране на епигенома е последвано от възстановяване на епигенетичните маркери и на транскрипционните профили, което позволява узряването на гаметите и в крайна сметка оплождането.
3. Глобалното метилиране на ДНК отново се изтрива след оплождането в ранните предимплантационни ембриони.
4. Накрая, с настъпването на клетъчната диференциация в пост-имплантационните ембриони, се извършва още един кръг на глобално метилиране de novo.
В експериментите, описани в статията по-долу, е показано, че е възможно да се преодолеят тези механизми (1-4) и епимутацията се запазва в поколенията.
CGI острови: цитозин-фосфат-гуанин богати сегменти (острови) от ДНК, които се намират често свързани с промоторни участъци пред активни гени ( и с това помагат за инициация на генната експресия). Тези острови са в не-метилирано състояние, за разлика отсилно метилираната ДНК в генома на млекопитаещите. са в неметилирано състояние. Свързаните с CGI промотори остават неметилирани през развитието и живота на организмите. Метилирането им води до подтискане на генната активност.
Въведение:
Пред много гени има промоторни участъци, направляващи началото на транскрипция. Те са богати на гуанинови и цитозинови нуклеотиди и оформят така наречените CpG острови - CGI. Характерно за CGI в и пред промоторите е, че не са метилирани. В противен случай транскрипцията би била потисната. Това не-метилирано състояние трябва да се поддържа, за да има активна транскрипция на гените след тези CGI острови. За целта съществува защитен механизъм срещу метилирането.
Протеини, притежаващи аминокиселинния мотив CXXC (Cys-X-X-Cys, където X е всяка аминокиселина) така наречените “цинкови пръсти”, предпазват островите CGI от de novo метилиране. Протеинът (TET1), който катализира превръщането на 5-метилцитозин в 5-хидрокси-метилцитозин, съдържа такъв CXXC мотив и се локализира в неметилираните острови CGI.
Друг CXXC протеин (CFP1) привлича комплекса Set1 към CGI островите, където Set1 катализира метилирането на хистон H3 на лизин 4 (H3K4).
Триметилираният лизин H3K4 (H3K4me3) обикновено се свързва с активна транскрипция и потенциално инхибира метилирането на ДНК, като предотвратява привличането de novo на ДНК-метилтрансферази към “без-метилните” острови CpGI.
Предполага се, че само механизмите за блокиране на метилирането не са достатъчни, за да се създадат и стабилно да се поддържат неметилирани островите CGI. Свързването на транскрипционни фактори и самите транскрипти вероятно също играят роля. Все още обаче не е известно как механизмът за блокиране на метилирането си сътрудничи с активния процес на транскрипция, за да установи и поддържа неметилиран статус на CGI.
В предишна своя работа Такахаши и сътр. установяват, че когато вземат едно парче/сегмент ДНК без CG (CpG free DNA) и го вмъкнат вътре в един промоторен остров (CGI) остров, в този остров се индуцира метилиране на ДНК (запълнените кръгчета в долната фигура 2). Това води до инхибиране на транскрипцията на гена (червения X в стрелката при началото на транскрипция TSS).
Може да предположим, че вмъкването на ДНК фрагмента нарушава целостта на CGI и предпазителите/защитниците срещу метилирането на CGI в този участък (споменати по-горе) не могат да си свършат работата.
Странното е, обаче, че ако се извади този вмъкнат сегмент, с което се възстановява нуклеотидната структура на “острова’, метилирането на острова се запазва и транскрипцията на гените след острова остава потисната. Химерни мишки, носещи тези промени, имат специфичен фенотип. В конкретния случай, гените след GCI са свързани с метаболизма - Ankrd26 и Ldlr.. Инхибирането на активността на тези гени, поради метиране на C и G води съответно до затлъстяване и хиперхолестеролемия.

|
(Фиг. 1) Когато тази генетична манипулация (може да я наречем метилиране чрез редактиране на ДНК), се извърши с ембрионални стволови клетки (ESCs) промененото епигенетично (метилирано) състояние се запазва стабилно при множество клетъчни деления в миши ESCs, дори след отстраняване на вмъкнатите ДНК сегментите). Поразително е, че трансгенните мишки, произведени с тези стволови клетки, запазват нивата на метилиране на изходните стволови клетки. Още по-забележително е, че това променено епигенетично състояние оцелява до известна степен (по-малко запълнени кръгчета- метилирани G и C) и в родителските полови клетки (germ cells), предава се след имплантация на зародиша, и се възстановява напълно (ср. увеличаване на броя (от две на четири) на запълнените кръгчета; (по-горе - фигура 1- долу вдясно) в потомството, и това се запазва през поколенията (F1 до F3), заедно със свързаните с това метаболитни фенотипи. Кредит: Cheng и сътр. (2) https://doi.org/10.1016/j.cell.2023.01.023 |
РЕЗЮМЕ:
ДНК метилирането на свързани с промотор CpG острови (CGI) може да се предава от родители на тяхното потомство при мишки. Редактирането на ДНК в миши ембрионални стволови клетки (ESCs) така, че да се метилират специфично CGI в промоторите на два свързани с метаболизма гени - Ankyrin26 (Ankrd26) и липопротеиновият рецептор с ниска плътност (LDL- receptor), довежда до потискане на активността на тези гени. Мишки, генерирани чрез микро-инжектиране на тези редактирани стволови клетки, показват анормални метаболитни фенотипове.
Придобитото метилиране на CGI островите и свързаните с това фенотипни черти се поддържат и предават през поколенията. Наследственото метилиране на CGI преживява препрограмирането в първичните полови клетки (primordial germ cells - PGC) и впоследствие e възстановено в следващото поколение на етапите след имплантиране.
Тези наблюдения демонстрират трансгенерационно епигенетично унаследяване при бозайници, което може да има отражение върху разбирането ни за еволюционната биология, както и за етиологията, диагностиката и превенцията на негенетично унаследявани човешки заболявания.

| (Фиг. 2) Фигура обобщаваща изследването: Трансгенерационно наследяване на придобити промени в метилирането на ДНК (1)
- Насочено метилационно ДНК-редактиране на CpG островите (CpGI) в миши ембрионални стволови клетки (ESC) в промоторния участък на гените Ankrd26 и Ldlr. Вмъкването на сегмент от ДНК без CpG предизвиква ДНК метилиране, което остава стабилно и след отстраняването на сегмента. - Мишки получени от метилационно - редактираните стволови клетки показват фенотипни промени, предизвикани от заглушаване на гените - затлъстяване и хиперхолестеролемия - Както придобитото метилиране, така и свързаните с това фенотипи се предават в множество поколения чрез половите клетки по бащина и майчина линия - Наследствената епигенетична памет възстановява метилирането на CрGI в епибластния стадий на зародиша. Кредит: Taкахаши и сътр. https://doi.org/10.1016/j.cell.2022.12.047 |
Накратко Takahashi и сътр. демонстрират, че инженерните епигенетични модификации и свързаните с тях фенотипове могат да се предават в множество поколения бозайници.
Генериране на редактирани с метилиране на ДНК миши стволови клетки (mESCs)

|
(Фиг. 3) (A–C и H) Схема на редактиране на метилирането на ДНК в CG остров (ограден в зелено) в ESCs. (A) Интегрирането/вмъкването на ДНК сегмент без CpG (CpG free - в жълто) в CGI индуцира de novo ДНК метилиране на целия CGI. Метилирането се поддържа стабилно и след отстраняването на този сегмент (запълнените кръгчета са метилирани нуклеотиди). (B, C) Насочено вмъкване, с помощта на нуклеаза Cas9 (насочена към средата на CGI чрез sgRNA по метода CRISPR), на сегмент от ДНК , в която няма CpG (CpG-free , ограден в жълто), вътре в островите CGI (означени в зелена рамка). Това индуцира ново метилиране в целия CGI. В краищата на сегмента са добавени специфични секвенции ТТАА и ААТТ с цел хомоложно рекомбиниране, както и ITR секвенции. Впоследствие този свободен от CpG сегмент се изрязва с PiggyBac транспозаза(активирана само временно и притежаваща само функция “скъсване”), която разпознава ITR и ТТАА и изрязва вмъкнатия преди това сегмент. (D, E, I, J) Анализ чрез бисулфитно секвениране. (D и I) - Всяка резка означава степента на метилиране на отделено CpG място в клонове ESC с вмъкнат сегмент - HR, или с изрязан след това сегмент - HRex. (E and J) Средна степен на метилиране за 18-те CpG места в CGI. (F) Диференциално метилиране - сравнение на наивните миши WT ESC и клонове HRex по цялата дължина около CGI. Явно е, че няма артефактно увеличено метилиране в областите извън CGI (т.е. само CGI се метилира). (G) Количествен RT-PCR анализ на експресията на Ankrd26 РНК. (K) Завишено метилиране(в червено) на CGI в Ldlr се запазва в клоновете Ldlr HR1ex (от тях е премахнат вмъкнатия сегмент) в CGI, без да е повлияно на околните нуклеотиди (в синьо). Кредит: Такахаши и сътр.(1) https://doi.org/10.1016/j.cell.2022.12.047 |

|
(Фиг.4) Генериране на химерни мишки с ДНК редактирано-метилиране на CGI (A) Схема на генериране на химерни мишки от редактирани с ДНК-метилиране mESC чрез микроинжектиране. (B) поколения затлъстяващи мишки с променен Ankrd - c1, c3 и спрямо дивия тип WT на възраст 10 месеца. Състояние на метилиране на 18 места от CpG острова - C, D, J, K, M и N) (D, K и N). (D и N) Статус на метилиране - сумарен анализ (вляво) и след анализ на TTAA алелите (вдясно). (E и O) Състояние на метилиране на целия CpG oстров - (Ankrd и Ldlr мишките съответно) - под абсцисната линия (в синьо) означава степен на не-метилиране, над линията (в червено)- на Ме+ метилиране. (F) Количествен RT-PCR анализ на експресията на Ankrd26 mRNA. (G) Телесно тегло на затлъстелите мъжки Ankrd химери спрямо мъжки ICR WT див тип мишки. (H) Серумни нива на лептин в WT мишки спрямо Ankrd химери. (I) Ankrd SL c1 мишка на 12-седмична възраст. (L) Ldlr c1 мишка на възраст 16 седмици. Вижда се, че изменение(увеличение) има в метилирането при химерните мишки само в областта на островите GCI, загубва се метилирането на хистона H3K4Me3, и отрицателно се влияе на транскрипцията и транслацията на гените (Ankdr4 и Ldlr) след метилираните острови. Съответни промени се наблюдават в теглото на мишките и серумнитеСъответни промени се наблюдават в теглото на мишките и серумните лептин (за Аnkrd26 мишките) и холестерол (за Ldlr мишките). Кредит: Takahashi et al https://doi.org/10.1016/j.cell.2022.12.047 |
Метилирането на CGI преминава през епигенетично препрограмиране в половите клетки и след оплождането се възстановява в ембрионите (вж. фиг. 5). При мишки се наблюдава пълно деметилиране, което започва в първичните половите клетки (primordial germ cells) около ден 8.5(Е8.5) и стига до метилиране под 10% при Е13.5. На същия стадий соматичните клетки в стадий Е13.5 са наследили метилираното състояние, за разлика от първичните зародишни клетки (гонади), които са с изчистено метилиране. Това не пречи в зародиша метилирането на CGI да е възстановено.
След оплождането започва глобално деметилиране на ДНК, което продължава до бластоцистния стадии (Е3.5). След това се извършва мащабно реметилиране на ДНК в пост-имплантационния зародиш. Кога се възстановява метилирането на CGI за Ldlr се установява от резултатите, показани на фиг. 5. Епибластите показват метилиране за разлика от бластоцистите (фиг 5 E).

| (Фиг. 5) Придобитото CGI ДНК метилиране се де-метилира в първичните зародишни клетки и се възстановява след това в епибластите.
(А) Схема на разделяне на препаратите в първичните зародишни клетки(primordial germ cells. PGC), гаметите и ранните зародиши. Е3.5 бластостоцисти; Е6.5-епибласти;мъжки, женски, мишки с инженирани CGI на Ankrd26 и Ldlr. (B, C, E, F, G, and J) Анализ на метилирането чрез бисулфитно секвениране за 18те CpG места в CGI на Ldlr (B, C, and E) и Ankrd26 (F, G, and J). (D and H) Метилирането в по-широка област около CGI - соматичните клетки са с възстановено метилиран , докато спермалните- не. (I) Метилационният статус на спермалните от дивия алел спрямо хомозиготните ТТАА алели. Проценти метилирана ДНК във всички проби. (K) Схема показваща динамиката на ДНК метилирането по целия геном и постигнатото ДНК метилиране на CGI по време на живота на мишките (две поколения F1 i F2). Докато ендогенните CGI остават неметилирани(зелена линия близо до абсцисата), придобилите насочено метилиране CGI стабилно се поддържат в това състояние в соматичните клетки (червена линия;виолетова линия) и го предават на поколението. CGI метилирането се изтрива в първичните зародишни клетки (PGCs) ( червена линия и жълта линия с минимум към Е13.5, поддържан по време на оплождането), и се възстановява в епибластите. Кредит: Takahashi et al https://doi.org/10.1016/j.cell.2022.12.047 (1) |
Да обобщим: Макар, че метилирането на Ldlr CGI островите се изтрива в зародишните клетки, неметилираните сперма и овоцити от соматично метилираните мишки могат да предадат паметта за метилиранаа ДНК на следващото поколение, и с това да възстановят метилирането на островите CGI, с което става предаване на Ldlr GCI островите през поколение - тоест имаме трансгенерационно унаследяване на епигенетична модификация (епимутация).
Изтриването на метилирането в зародишния стадий, последвано от възстановяването му на по-късни етапи, представлява една загадка. Не е ясно какъв ще е механизма за запазване на тази памет. Да си представим унаследяване на метилирането в соматични клетки не е трудно. При репликация на ДНК новите вериги са хеми-метилирани, тоест носят наполовина от белезите на метилирането. Не е трудно да си представим как към тези белези могат да бъдат привлечени метилиращи фактори (метилтрансферази и др.), които да довършат метилирането на останалата половина неметилирана ДНК. Въпросът как се предава метилирането след изтриването на паметта в гаметите остава обаче без отговор в това изследване.
Евентуални кандидати за някакъв механизъм на предаване на тази епигенетична информация са некодиращи РНK и белтъците от поликомб групата (вж. още по-темата (1) и (2)). Унаследяване на метилирането със следващите го фенотипни промени е рядко явление, но е пример за унаследяване на придобит белег (а ла Ламарк).
Разкриването на факторите, участващи в този епигенетичен процес ще доведе до напредък в изясняване на макро-еволюцията, на ембриогенезата при млекопитаещите, и в крайна сметка ще разкрие стратегии за лекуване на свързани с метилирането заболявания.
Справка:
1.Takahashi et al.Transgenerational inheritance of acquired epigenetic signatures at CpG islands in mice, Cell, 186, 715–731 2023 https://doi.org/10.1016/j.cell.2022.12.047
2.Saifeng Cheng, Yoav Mayshar, Yonatan Stelzer Induced epigenetic changes memorized across generations in mice, Cell 186,, 683-685, 2023 https://doi.org/10.1016/j.cell.2023.01.023
Подбор и обсъждане - Константин К. Чипев, PhD в Ню-Йоркския Щатски У-тет в Стони Брук.
Още по темата:
(1). “Епигенетично онаследяване на активирано хроматиново състояние”
(2). “Майките осигуряват успеха на поколението си чрез епигенетика”
Още по темата

Животът
Ембрионите нулират биологичния си часовник 5 - 10 дни след зачеването
Медицина
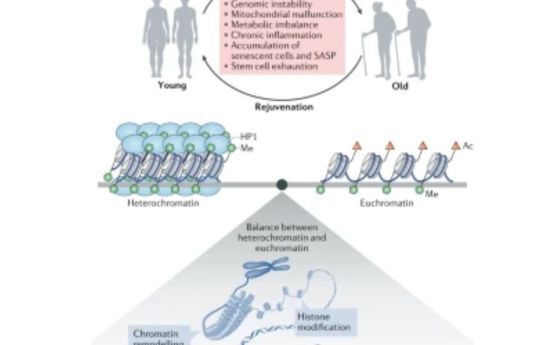
Стареещият епигеном и как да го подмладим

Медицина
Тренировките могат да променят самите молекули в човешкото тяло, които влияят на поведението на гените

















Коментари
Моля, регистрирайте се от TУК!
Ако вече имате регистрация, натиснете ТУК!
Няма коментари към тази новина !
Последни коментари